Sur cette page
- 1. Objectif
- 2. Exigences concernant l'importation ou la dissémination d'engrais et de suppléments au Canada
- 3. Effectuer des essais à des fins de recherche en vertu de la Loi sur les engrais
- 4. Critères pour les essais à des fins de recherche
- 5. Exemptions s'appliquant aux essais en milieu fermé et dérogation de recherche
- 6. Exemptions de l'obligation de détruire la récolte
- 7. Aperçu du processus lié aux autorisations de recherche
- 8. Catégories d'autorisation de recherche
- 9. Documentation exigée selon la catégorie d'autorisation de recherche
- 9.1 Formulaire de demande
- 9.2 Étiquette pour usage expérimental
- 9.3 Cartes du lieu de l'essai
- 9.4 Plan expérimental
- 9.5 Constituants
- 9.6 Inoculum microbien
- 9.7 Processus de fabrication et procédures de contrôle de la qualité
- 9.8 Élimination des récoltes et des produits
- 9.9 Justification supportant l'innocuité
- 9.10 Caractérisation des dangers microbiens
- 9.11 Caractérisation de l'exposition
- 9.12 Caractérisation microbienne
- 9.13 Microorganismes modifiés par des techniques de biologie moléculaire
- 9.14 Plan et procédure de surveillance
- 9.15 Procédures de confinement
- 9.16 Plan d'urgence
- 10. Inspection
- 11. Dossiers et communication de données
- 12. Coordonnées
- Annexe A : Exemples de cartes acceptables
1. Objectif
L'objectif du présent document est de décrire les exigences concernant les engrais et les suppléments importés ou fabriqués au Canada à des fins expérimentales. Il fournit également des conseils en ce qui a trait au processus d'obtention des autorisations de recherche pour les suppléments nouveaux en vertu de la Loi sur les engrais et son règlement d'application.
2. Exigences concernant l'importation ou la dissémination d'engrais et de suppléments au Canada
Loi sur les engrais, 2.1 Interdiction générale :
Il est interdit de fabriquer, vendre, d'importer ou d'exporter tout engrais ou supplément qui contient une substance ou un mélange de substances en des quantités qui présentent un risque de préjudice à la santé humaine, animale ou végétale ou à l'environnement, à l'exception des parasites, si l'engrais ou le supplément est utilisé selon son mode d'emploi ou appliqué en une quantité qui ne dépasse pas la quantité nécessaire pour atteindre l'objectif visé.
La plupart des suppléments et certains engrais doivent faire l'objet d'un enregistrement et d'une évaluation préalable à la mise en marché avant de pouvoir être importés ou vendus au Canada. Les entreprises choisissent parfois d'effectuer des essais à des fins de recherche sur des engrais ou des suppléments afin d'évaluer leur efficacité sur le terrain avant de présenter une demande d'enregistrement d'un produit en vertu de la Loi sur les engrais. Le Règlement sur les engrais renferme des dispositions qui permettent à des personnes de procéder à des essais scientifiques sur des engrais et des suppléments non enregistrés qui devraient normalement être enregistrés avant d'être importés ou disséminés, si des critères stricts sont respectés.
Les exigences réglementaires qui s'appliquent actuellement à la recherche visent à assurer la dissémination sécuritaire d'engrais non enregistrée (non exemptés de l'enregistrement) et de suppléments nouveaux et à définir les conditions liées à l'utilisation des produits, à leur manipulation et à leur élimination afin de réduire les risques pour la santé humaine et animale et l'environnement.
Dans certains cas, un permis d'importation délivré par l'ACIA est aussi exigé. Veuillez consulter le Système automatisé de référence à l'importation (SARI) pour déterminer s'il y a d'autres exigences relatives à l'importation.
3. Effectuer des essais à des fins de recherche en vertu de la Loi sur les engrais
3.1 Effectuer des recherches sur les engrais
Un engrais importé ou fabriqué au Canada à des fins expérimentales doit être sûr (article 2.1 du Règlement), mais peut être soustrait des exigences liées à l'enregistrement et à l'étiquetage si :
- le produit ne contient pas un supplément ou un pesticide;
- tout le matériel végétal traité et les produits résiduels sont détruits à la fin de l'essai afin d'éviter qu'ils n'entrent pas dans les chaînes commerciales d'alimentation humaine ou animale.
Dans le cadre des essais à des fins de recherche menés sur des engrais qui sont actuellement enregistrés pour un autre usage (par exemple, plantes ornementales par rapport aux cultures vivrières agricoles), tout le matériel végétal traité doit également être éliminé à la fin de l'essai afin d'empêcher leur entrée dans les chaînes commerciales d'alimentation humaine ou animale.
Les exigences concernant la recherche sur les engrais qui contiennent des suppléments sont les mêmes que pour les suppléments nouveaux. Veuillez consulter les sections 3.2 et 3.3.
3.2 Effectuer des recherches sur les suppléments
Les essais à des fins de recherche sur des suppléments qui sont exemptés de l'enregistrement ou qui sont déjà enregistrés en vertu de la Loi sur les engrais, lorsqu'ils sont menés conformément au mode d'emploi approuvé, peuvent être réalisés sans avoir obtenu l'approbation de l'ACIA. Cependant, si l'utilisation ou le mode d'emploi du produit mis à l'essai ne correspond pas à ce qui a été approuvé, une autorisation de recherche est requise avant de procéder à l'essai. Ces types d'autorisations sont équivalents aux essais avec des suppléments nouveaux. Voir la section 3.3 pour obtenir des renseignements détaillés.
Loi sur les engrais, Définitions et interprétation :
Un supplément nouveau signifie, selon le cas :
- d'un supplément non enregistré et non exempté de l'enregistrement;
- d'un supplément issu de la biotechnologie et doté d'un caractère nouveau.
Un caractère nouveau signifie un caractère d'un supplément issu de la biotechnologie qui
- d'une part, a été intentionnellement sélectionné, créé ou incorporé dans une population distincte et stable de suppléments de la même espèce par une modification génétique particulière;
- d'autre part, en ce qui a trait à son usage particulier et à son innocuité tant pour l'environnement que pour la santé humaine, sur la foi d'une justification scientifique valable, n'est essentiellement équivalent à aucun caractère d'un supplément semblable qui, au Canada, est déjà employé comme supplément et considéré comme étant sans risque.
3.3 Autorisations de recherche pour des suppléments nouveaux
Les autorisations de recherche visent à assurer la dissémination sécuritaire du supplément nouveau. Elles prescrivent des conditions de confinement, l'équipement de protection et les méthodes d'élimination des récoltes. Les exigences et le processus pour soumettre une demande d'autorisation de recherche sont décrits en détail dans les sections ci-dessous.
4. Critères pour les essais à des fins de recherche
Tous les essais effectués sur des suppléments nouveaux au Canada doivent satisfaire aux critères généraux suivants :
- Les essais doivent être effectués par un chercheur qualifié, à l'aide de méthodes scientifiques valides. Le ou les chercheurs responsables des essais sur le terrain doivent au moins avoir un baccalauréat en agriculture ou dans un domaine scientifique connexe ou posséder l'expérience de la réalisation d'essais scientifiques sur le rendement d'un produit agricole.
- Les bonnes pratiques de laboratoire et les procédures de contrôle de la qualité appropriées doivent être suivies. L'entreprise ou l'institut de recherche n'ont pas nécessairement besoin d'être certifiés comme employant les bonnes pratiques de laboratoire.
- L'établissement de recherche doit assurer la sécurité de ses employés durant l'essai.
- La recherche doit être effectuée dans des endroits où le supplément n'est pas susceptible de s'échapper (par exemple, par ruissellement, érosion, dérive, lessivage, etc.); et où l'exposition des passants au supplément ou au sol ou aux végétaux traités est limitée.
- Les plantes traitées, les milieux de croissance et le produit inutilisé ne doivent pas être vendus ni distribués et tous les suppléments, engrais et matériel végétal, y compris les cultures récoltées, provenant des sites traités doivent être éliminés en toute sécurité à la fin des essais, sauf si une exemption de l'obligation de détruire la récolte a été accordée par l'ACIA (voir ci-dessous pour de plus amples renseignements). Les requérants doivent proposer une méthode d'élimination sécuritaire, qui peut varier en fonction de la nature du supplément (microbien par rapport à chimique), la probabilité de sa propagation et de son établissement dans l'environnement ainsi que le risque relatif rattaché à la dissémination. Pour plus de conseils sur les méthodes sécuritaires d'élimination de la récolte, veuillez communiquer avec nous.
5. Exemptions s'appliquant aux essais en milieu fermé et dérogation de recherche
Les essais de recherche où la dissémination du supplément dans l'environnement est impossible, tels que les essais en milieu fermé (laboratoires par exemple), ne nécessitent pas d'autorisation de recherche tant que des mesures appropriées sont mises en place pour empêcher la libération dans l'environnement. Les recherches effectuées en serre peuvent être considérées comme étant en milieu fermé ou non. Pour être considérées comme un milieu d'essai fermé, les conditions de la serre doivent être adéquates pour empêcher la dissémination et la propagation du supplément dans l'environnement.
Les requérants souhaitant être exemptés de l'obligation d'obtenir une autorisation de recherche doivent donc présenter une demande afin d'obtenir une dérogation de recherche. Pour ce faire, ils doivent notamment fournir :
- le nom du supplément ou de l'engrais. Cela comprend la liste des ingrédients, leurs sources, leur concentration, les garanties et les Fiches de données de sécurité;
- le but et l'objectif de la recherche;
- la date de début des recherches proposée;
- l'espèce de végétaux qui sera traitée;
- la quantité totale de produits nécessaire ou importée aux fins de la recherche, y compris les taux et les méthodes d'application;
- les détails du plan de destruction des végétaux traités et du produit à la fin de l'essai;
- tout autre renseignement pertinent à l'innocuité du produit. Cela peut comprendre une évaluation des risques et une description de l'équipement de protection individuelle à porter pour manipuler le produit;
- le nom, l'adresse complète et une description détaillée de l'installation où les essais du produit seront effectués. Cela comprend la description des systèmes de traitement de l'air, de l'eau et des effluents;
- la description des secteurs traités, les caractéristiques d'isolement et les marches à suivre pour l'isolement des zones de recherche;
- les pratiques de manipulation de prévention de la dissémination accidentelle du produit dans l'environnement;
- l'énoncé des compétences et de la formation du personnel.
Les conditions de confinement de chaque installation sont examinées au cas par cas par l'ACIA et, si cela est jugé approprié, l'exemption est accordée. Si vous avez des questions sur la classification de votre installation, veuillez communiquer avec nous.
6. Exemptions de l'obligation de détruire la récolte
L'ACIA peut accorder une exemption de l'obligation de détruire la récolte si l'innocuité a été évaluée de façon appropriée (identifiée comme étant une évaluation des données avec une justification d'innocuité ou DS) et si le supplément ou l'engrais a été jugé sans danger lorsqu'il est utilisé selon le mode d'emploi.
L'évaluation de l'innocuité doit être complétée par l'ACIA avant de demander l'autorisation de recherche et l'exemption susmentionnée. Les évaluations complètes de l'innocuité en vue d'obtenir l'exemption de détruire la récolte seront placées dans la file d'attente de l'examen des dossiers et elles ne seront pas accélérées. La norme de prestation des services de l'ACIA dans le cas d'une DS est équivalente à un nouvel enregistrement avec données, qui se trouve dans la Circulaire à la profession T-4-122.
Les requérants ayant reçu une exemption de l'obligation de détruire la récolte peuvent :
- effectuer des essais à l'échelle de la ferme (plus d'un hectare);
- utiliser les champs des agriculteurs par opposition aux installations de recherche pour effectuer les essais;
- utiliser ou vendre les récoltes traitées. Veuillez noter que les exemptions de l'obligation de détruire la récolte n'autorisent pas la vente ou la distribution du supplément ou de l'engrais lui-même.
7. Aperçu du processus lié aux autorisations de recherche
7.1 Présenter une demande
Les nouvelles demandes d'autorisation de recherche peuvent dorénavant être soumises par l'entremise de la plateforme électronique (Mon ACIA). Les requérants sont fortement encouragés à utiliser Mon ACIA. Bien que les demandes soumises par courriel ou par la poste sont acceptées, elles prennent plus de temps à traiter et ne sont donc pas le moyen privilégié par l'ACIA en ce qui a trait au traitement des dossiers.
La plateforme de prestation numérique des services Mon ACIA vous permet de demander des services, de les payer et de suivre l'état de votre demande en ligne en tout temps, peu importe où vous vous trouvez, par l'entremise d'un compte sécurisé qui peut être personnalisé en fonction de votre modèle d'affaires. Pour présenter une demande d'autorisation de recherche en ligne, vous devez d'abord créer un profil dans Mon ACIA. Vous verrez ensuite la liste des services disponibles, notamment ceux du Bureau de présentation des demandes préalables à la mise en marché pour une autorisation de recherche. Les documents d'orientation, les vidéos et les directives détaillées pour créer et gérer votre compte et demander des services en ligne se trouvent à l'adresse Mon ACIA – Orientation de l'utilisateur.
Si vous choisissez de présenter une demande par courriel ou par la poste, veuillez envoyer les renseignements exigés au Bureau de présentation des demandes préalables à la mise en marché. Lorsque vous présentez une demande par la poste, il est préférable qu'elle soit soumise (le plus possible) en format électronique (CD-ROM, DVD, clé USB) pour faciliter le traitement rapide de votre demande.
Les renseignements exigés sont les mêmes, que la demande soit présentée par voie électronique ou sur papier.
7.2 Dates limites pour la présentation des demandes
Les demandes doivent être soumises au moins 90 jours avant la date du début des essais. La norme de prestation de services de 90 jours correspond au délai de traitement par l'ACIA uniquement et ne tient pas compte du temps écoulé entre la réception de la demande et le paiement, ni du temps pendant lequel le demandeur prépare une réponse à une demande de clarification/de renseignements supplémentaires de l'ACIA.
7.3 Processus d'examen des demandes
Tous les requérants qui désirent obtenir une autorisation de recherche doivent remplir le formulaire de demande (CFIA/ACIA 5475) qui fournit des renseignements sur les essais et le produit visé. Les requérants doivent soumettre tous les renseignements exigés, comme il est indiqué ci-dessous, en fonction de la catégorie de recherche (une description de chaque catégorie est incluse dans la section 8). Lorsqu'elle recevra la demande, l'ACIA confirmera la catégorie d'autorisation de recherche et le requérant sera informé par écrit de la décision et des frais qui s'y rattachent (lien à l'avis des frais). Cette étape du processus d'examen sera terminée au plus tard 30 jours après la réception de la demande.
Une fois que le règlement des droits est reçu et que les renseignements fournis répondent aux exigences du Règlement, l'étape suivante de l'examen commence. L'ACIA fournira alors une ébauche de l'annexe de l'autorisation de recherche au requérant afin de s'assurer de l'exactitude des renseignements et de confirmer que l'autorisation de recherche reflète le plan proposé pour les essais sur le terrain. Toute modification ou tout changement apporté par le requérant sera ensuite évalué par l'ACIA et l'autorisation de recherche sera finalisée.
Les requérants recevront par la suite une autorisation de recherche qui décrit les conditions spécifiques de l'essai. Les conditions indiquées dans l'autorisation doivent être respectées pendant toute la durée de l'essai. Dans le cas des renouvellements, les requérants recevront une autorisation de recherche qui décrit les mêmes conditions que celles prescrites l'année précédente (à moins que de nouveaux renseignements justifient une modification).
Toute modification à l'autorisation de recherche finale doit être soumise à l'ACIA aux fins d'approbation avant sa mise en œuvre. Cela comprend des changements au protocole de recherche comme le lieu de l'essai, la taille ou les méthodes d'élimination des cultures, etc.
7.4 Fréquence de la présentation des demandes d'autorisation de recherche
Pour toutes les catégories d'autorisation, un formulaire de demande doit être soumis pour chaque année de l'essai pour chacun des produits et des espèces cultivées ou des groupes de cultures.
Si le produit, la méthode d'essai et l'espèce ou le groupe de cultures sont les mêmes, les essais effectués à plusieurs endroits peuvent être indiqués dans la même autorisation de recherche. Si les requérants désirent inscrire plusieurs essais menés sur des récoltes du même groupe de cultures dans une seule demande, une justification valide sur le plan scientifique qui démontre la similarité des cultures doit être soumise, puis approuvée par l'ACIA. Cette justification doit comprendre des données probantes taxonomiques ou physiologiquement pertinentes, selon lesquels l'espèce cultivée dans le groupe réagira de manière semblable au supplément nouveau ou à l'engrais contenant un supplément nouveau soumis à l'essai.
8. Catégories d'autorisation de recherche
Catégorie A : Demande de recherche standard pour une nouvelle recherche
- Essai d'un supplément nouveau ou d'un engrais contenant un supplément nouveau qui pose un risque négligeable pour la santé végétale, animale et humaine, ainsi que pour l'environnement.
- Pourrait comprendre une évaluation de l'innocuité de niveau I, comme il est indiqué dans le Guide pour la présentation des demandes d'enregistrement, ou une nouvelle utilisation proposée (par exemple, un nouveau type de culture, modification du mode d'emploi) pour des produits qui ont déjà fait l'objet d'un examen par l'ACIA pour une entreprise donnée.
Catégorie B : Demande de recherche pour une nouvelle recherche en plus d'un examen des données d'innocuité
- Essai d'un supplément nouveau ou d'un engrais contenant un supplément nouveau non encore évalué par l'ACIA, génétiquement modifié ou qui présente un risque potentiel ou inconnu pour la santé humaine, animale, végétale ou pour l'environnement.
- Pourrait comprendre une évaluation de l'innocuité de niveau II et III, comme il est indiqué dans le Guide pour la présentation des demandes d'enregistrement.
- Si elle le juge nécessaire, l'ACIA pourrait imposer des conditions spécifiques pour atténuer le risque, ou refuser d'autoriser l'essai.
Catégorie C : Renouvellement d'une autorisation de recherche
- Réservé aux renouvellements d'autorisations de recherche déjà accordées.
- Comprends la surveillance d'un site d'essai sans nouvelle application du produit et les années ultérieures d'essai du même produit sur le même groupe d'espèce cultivée.
- Des sites d'essais additionnels peuvent être ajoutés à la demande du requérant.
- Une nouvelle autorisation de Catégorie C est nécessaire pour chaque année civile de la durée de l'essai.
- Dans le cas de la Catégorie C, une déclaration signée par le chercheur responsable ou le requérant, indiquant que tous les paramètres de l'essai sont les mêmes que dans l'autorisation précédemment accordée, est requise.
9. Documentation exigée selon la catégorie d'autorisation de recherche
Pour demander une autorisation de recherche, tous les requérants doivent soumettre des documents à l'ACIA selon la catégorie de l'autorisation de recherche.
- Catégorie A : Sections 9.1 à section 9.8 inclusivement, dans la mesure où elles s'appliquent au produit visé
- Catégorie B : Sections 9.1 à section 9.16 inclusivement, dans la mesure où elles s'appliquent au produit visé
- Catégorie C : Sections 9.1 à section 9.3 inclusivement
9.1 Formulaire de demande
Tous les requérants doivent remplir le formulaire de demande d'autorisation de recherche (CFIA/ACIA 5475). Le formulaire doit être rempli au complet et signé par le requérant et le chercheur responsable.
9.2 Étiquette pour usage expérimental
Une étiquette pour usage expérimental ou une fiche d'information doit accompagner le produit mis à l'essai et doit être jointe au formulaire de demande. L'objectif de l'étiquette pour usage expérimental ou de la fiche d'information est de s'assurer que les préposés à l'application du produit recevront les consignes appropriées concernant l'utilisation, la manutention et l'élimination. Ces étiquettes ou fiches doivent également être fournies au chercheur responsable et être mises à la disposition de tous les travailleurs qui participeront directement à l'essai. Une fois approuvées par l'ACIA, l'étiquette pour usage expérimental ou la fiche d'information doivent être apposées sur les récipients du produit à utiliser pendant l'essai. Les renseignements devraient être dactylographiés lisiblement dans les deux langues officielles et ils devraient correspondre au mode d'emploi à appliquer dans l'éventuel projet de recherche.
Les renseignements ci-dessous doivent figurer sur l'étiquette pour usage expérimental ou la fiche d'information accompagnant le produit.
Mentions obligatoires :
- Lire l'étiquette avant l'emploi
- Pour usage expérimental seulement
- La vente de ce produit est interdite.
- Ne pas distribuer à une personne autre qu'aux chercheurs ou à leurs collaborateurs
- Tout produit inutilisé doit être retourné au fabricant, à moins que des méthodes appropriées de stérilisation n'existent.
Renseignements obligatoires :
- Nom et identificateur du produit
- Nom et adresse du fabricant
- Contenu net
- Ingrédient actif et sa concentration ou garantie
- Mode d'emploi, y compris l'espèce cultivée, la méthode d'application et la dose d'application
- Méthode de nettoyage ou de stérilisation
- Méthode d'élimination de la récolte (dois correspondre à la méthode précisée dans l'autorisation de recherche)
- Nom et coordonnées du chercheur responsable et du collaborateur
Ajouter, le cas échéant :
- Consignes d'entreposage et date de péremption
- Élimination du produit
- Avertissements et précautions à prendre
- Renseignements sur les premiers soins
- Équipement de protection individuelle à porter pendant le transport, le mélange, le chargement, l'application, l'élimination et le nettoyage du produit renversé
9.3 Cartes du lieu de l'essai
Il est de la responsabilité du requérant de fournir à l'ACIA la localisation géographique du site d'essai, y compris les descriptions de terrain légales et les cartes détaillées.
Les cartes de tous les lieux d'essai sur le terrain doivent être lisibles et précises, pour permettre aux inspecteurs de l'ACIA de situer l'essai, au cours de l'année et des années suivantes, au besoin. Les cartes devraient se trouver sur une page blanche, avec dessins au trait net et précis et lettres moulées. Les cartes dessinées sur papier ligné ou graphique ou les photocopies de cartes routières ou topographiques ne sont pas acceptées.
Les renseignements suivants doivent être clairement imprimés sur chaque carte :
- L'emplacement du lieu de l'essai (ville, province). Si l'essai a lieu à l'intérieur d'une ville, inclure l'adresse municipale. Sinon, inclure les distances et les directions par rapport à la ville la plus proche, de même que la description légale du terrain.
- La direction de compas, avec le nord au haut de la page.
- Les coordonnées géographiques (GPS) du site de l'essai et de trois repères environnants permanents. Si ceci est impossible, fournir un minimum de trois mesures distinctes à partir de deux points de repère proches jusqu'à deux des angles du lieu, au demi-mètre près, pour situer avec précision le lieu en question.
On peut également utiliser les coordonnées du système mondial de positionnement (GPS) pour marquer les limites extérieures du lieu de l'essai (par exemple, dans le cas d'une parcelle rectangulaire, ses quatre angles) et trois points de repère permanents des environs. Les points de repère permanents doivent se trouver dans un rayon de 10 km du terrain de l'essai. Si on se sert d'un immeuble ou d'un autre gros point de repère permanent, veuillez préciser quelle partie a servi de point de repère (par exemple, l'angle sud-ouest de la grange rouge). De plus, veuillez choisir des points de repère bien espacés (ne pas prendre trois mesures de référence à partir du même immeuble). À noter que les cartes sont requises même si le lieu de l'essai est localisé à l'aide de coordonnées GPS (lesquelles devraient être marquées sur la carte).
- Les dimensions exactes du lieu de l'essai et la description des cultures environnantes.
- Le nom et le numéro de téléphone de la personne-ressource sur le terrain.
- Le numéro de contrôle de la demande désigné par l'ACIA (exigé sur la carte finale seulement) et les traitements effectués à ce lieu d'essai.
- La date de la mise en place de l'essai.
Un exemple de carte acceptable (avec et sans coordonnées GPS) se retrouve à l'annexe A du présent document.
9.4 Plan expérimental
Une description du plan expérimental et du régime de traitement est exigée pour les essais de catégorie :
- demande de recherche standard pour une nouvelle recherche, et
- demande de recherche pour une nouvelle recherche en plus d'un examen des données d'innocuité
Cela comprend la taille totale de l'essai ainsi que la taille des parcelles individuelles, la description des traitements, le nombre de reproductions, le taux d'ensemencement et les détails particuliers aux taux et aux méthodes d'application du supplément nouveau. Afin d'atténuer la propagation du supplément nouveau ou de l'engrais contenant un supplément nouveau dans l'environnement, des zones tampons autour et entre les parcelles pourraient aussi être nécessaires.
9.5 Constituants
Tous les ingrédients doivent être identifiés, ainsi que leur source et leur concentration. Les fiches de données de sécurité devraient être fournies pour les ingrédients individuels ainsi que pour le produit final.
9.6 Inoculum microbien
Pour les produits qui contiennent des microorganismes viables d'origine naturelle, on doit fournir les renseignements suivants :
- l'objectif de la souche microbienne dans le produit;
- l'identification taxonomique du microorganisme au niveau de l'espèce et du genre; les renseignements concernant la sous-espèce et la souche (s'ils sont disponibles);
- les résultats analytiques appuyant l'identité et la classification taxonomique;
- les méthodes utilisées dans l'identification de tous les microorganismes retrouvés dans le produit final;
- les relations avec des agents pathogènes connus (arbres phylogénétiques);
- l'origine du microorganisme (l'endroit, le moment et la substance de laquelle il a été isolé). Si la souche a été déposée dans une souchothèque reconnue (par exemple, l'American Type Culture Collection ou autre, ou obtenue d'une telle source, il faut fournir les numéros d'accès.
9.7 Processus de fabrication et procédures de contrôle de la qualité
Il faut fournir une brève description du processus de fabrication accompagnée d'un graphique illustrant un aperçu du procédé, avec les procédures de contrôle de la qualité utilisées afin d'assurer une uniformité au niveau de la production et de la pureté du produit final. Si le requérant n'a pas accès à ces renseignements, le fabricant peut les fournir directement. Dans ce cas, les renseignements commerciaux confidentiels ne seront pas divulgués ou publiés à toute personne ou tout parti, y compris le requérant, sans l'autorisation écrite du fabricant.
9.8 Élimination des récoltes et des produits
Tout le matériel végétal, y compris les cultures récoltées des sites traités, doit être éliminé de façon sécuritaire à la fin de l'essai à moins qu'une exemption de l'obligation de détruire la récolte n'ait été accordée par l'ACIA. Les requérants doivent proposer une méthode d'élimination sécuritaire, avec une justification basée sur la nature du produit (microbien par rapport à chimique), la probabilité de sa propagation et de son établissement dans l'environnement ainsi que le risque relatif rattaché à la dissémination.
L'élimination des produits implique souvent le retour de tous les produits inutilisés au fabricant pour leur destruction conforme (autoclave, incinérateur, etc.).
Les méthodes de destruction des récoltes comprennent, sans toutefois s'y limiter : la collecte et la stérilisation de tout le matériel végétal traité, l'incinération, l'élimination à un site d'enfouissement, la récolte et l'incinération du matériel végétal résiduel sur le site, l'enfouissement en profondeur à une profondeur de plus d'un mètre, l'incorporation dans le sol, et l'élimination conforme aux règlements provinciaux et municipaux normaux.
9.9 Justification supportant l'innocuité
Une justification supportant l'innocuité, fondée sur des données expérimentales et/ou sur des publications scientifiques, doit être fournie pour le produit et tous ses ingrédients. Dans cette justification, veuillez identifier tout risque potentiel que pose le supplément nouveau ou l'engrais contenant le supplément nouveau pour la santé humaine et l'environnement, et discuter de toutes les études où on a signalé des effets nocifs de l'utilisation des matières actives.
À noter que l'évaluation de l'innocuité n'est pas considérée comme une « évaluation complète de l'innocuité » pour l'enregistrement du produit et sa commercialisation. Des renseignements supplémentaires peuvent être exigés au moment de l'enregistrement du produit ou pour accorder une exemption de l'obligation de détruire la récolte dans le cas de certains produits.
9.10 Caractérisation des dangers microbiens
En utilisant des données publiques ou primaires, veuillez aborder les paramètres de danger suivants :
- Humains : pathogénicité, toxicité, sensibilisation/irritation et potentiel dermatophytique
- Plantes et cultures terrestres : pathogénicité/toxicité, inhibition de la croissance
- Espèces non ciblées : mammifères, autres vertébrés terrestres (par exemple, oiseaux), invertébrés (par exemple, abeilles, vers de terre, collemboles), vertébrés aquatiques (par exemple, poissons), invertébrés (par exemple, benthique, épibenthique) et plantes aquatiques (par exemple, algues).
Les renseignements présentés devraient être assortis des références appropriées. Veuillez fournir un exemplaire de chaque publication ou rapport cité.
9.11 Caractérisation de l'exposition
Veuillez fournir une évaluation de l'exposition en abordant les facteurs suivants :
- Selon l'utilisation visée cultures/plantes ciblées, méthode d'application prévue, taux d'application, calendrier et fréquence de l'application, évaluations d'exposition directe et indirecte pour le scénario d'essai proposé
- Exposition directe : travailleurs/passants par des voies d'exposition cutanée, par inhalation et par ingestion.
- Exposition indirecte : voies d'assimilation par le sol, les eaux souterraines et les végétaux.
9.12 Caractérisation microbienne
Veuillez caractériser les microorganismes en fournissant les renseignements détaillés suivants (veuillez fournir les références pour tous les renseignements indiqués) :
Présence dans la nature
- Distribution géographique
- Habitats naturels : sols, eau, atmosphère, sur ou à l'intérieur d'organismes vivants (par exemple, endophyte, épiphyte)
- Hôtes (relations symbiotiques, saprophytiques ou pathogènes)
Description du cycle de vie
- Caractéristiques des différentes formes de microorganisme pendant le cycle de vie (par exemple, cellules motiles, kystes dormants, spores)
- Mécanisme de reproduction et de dispersion
- Mécanisme de survie (dans des conditions adverses)
Propriétés physiologiques
- Paramètres de croissance (par exemple, température, pH, propriétés osmotiques minimales, maximales et optimales)
9.13 Microorganismes modifiés par des techniques de biologie moléculaire
Pour les microorganismes modifiés par des techniques de biologie moléculaire, le requérant doit fournir les renseignements suivants :
- Un diagramme représentant le processus de modification génétique, avec ce qui suit :
- la carte de la construction génétique insérée dans l'hôte
- son emplacement (chromosome ou plasmide)
- le nombre d'exemplaires
- les vecteurs utilisés
- les séquences du promoteur
- les gènes marqueurs, y compris tout gène de résistance aux antibiotiques;
- La description détaillée des produits de la construction génétique, de leurs propriétés et de leurs fonctions;
- La description des voies métaboliques modifiées par l'insertion;
- Les effets non désirés sur l'expression des gènes (réduction ou augmentation de l'expression d'autres gènes);
- La stabilité du matériel génétique inséré;
- Le potentiel de transfert horizontal des gènes : capacité de transférer le matériel génétique inséré entre l'organisme hôte et des espèces non ciblées, les mécanismes de transfert possible (transformation, transduction ou conjugaison) et les éléments pris en compte (plasmides, bactériophages, éléments conjugatifs intégrateurs, transposons, séquences d'insertion, intégrons, cassettes de gènes et îlots génomiques);
- Les procédures et les analyses qui permettent de détecter et de quantifier les microorganismes modifiés.
Pour plus d'information sur la préparation d'une justification bien structurée et complète pour supporter l'innocuité, veuillez consulter l'onglet 5 du Guide pour la présentation des demandes d'enregistrement en vertu de la Loi sur les engrais.
9.14 Plan et procédure de surveillance
Un plan de surveillance de la propagation et de l'établissement du supplément nouveau ou de l'engrais contenant un supplément nouveau dans l'environnement durant l'essai doit être fourni. La méthode utilisée pour identifier et suivre la substance chimique ou le microorganisme nouveau doit être approuvée par l'ACIA avant la mise en œuvre de l'essai.
L'échantillonnage et le testage de parties de végétaux comestibles et non comestibles, dans les cas où le produit pourrait mener à des résidus dans/sur le végétal ou la récolte (par exemple, dans les cas de colonisation endophyte ou épiphyte, respectivement), peuvent aussi être nécessaires dans le cadre du plan de surveillance.
La dissémination de certains suppléments nouveaux et d'engrais contenant des suppléments nouveaux pour la recherche scientifique pourrait exiger que le lieu de l'expérience soit surveillé après la fin de l'essai. En pareil cas, les protocoles d'échantillonnage et les méthodes d'analyse utilisées pour déceler et surveiller la persistance du produit dans l'environnement doivent être approuvés par l'ACIA avant la mise en place de l'essai. Une fois approuvés, le plan et les modes opératoires de la surveillance doivent faire partie de l'autorisation de recherche en tant que l'une des conditions de la dissémination.
Si, à quelque moment que ce soit, après ou pendant la réalisation des travaux de recherche, on détermine que la dissémination du produit a des effets néfastes sur la santé végétale, animale et humaine ou sur l'environnement, des mesures appropriées telles que la fumigation du sol ou le contrôle des modes d'utilisation des sols après la récolte devront être mis en œuvre, aux frais du requérant et/ou du chercheur responsable.
9.15 Procédures de confinement
Une description détaillée des procédures de confinement visant à atténuer l'établissement et la dissémination du supplément nouveau ou de l'engrais contenant un supplément nouveau dans l'environnement doit être soumise pour les essais de recherche effectués en serre ainsi que sur le terrain. Ceux-ci comprennent, sans s'y limiter, des descriptions de l'emballage du supplément pendant l'expédition et l'entreposage, le calendrier et les méthodes d'application, l'aménagement de zones tampons (au besoin), le contrôle de l'entrée dans le périmètre de recherche, ainsi que le nettoyage et la stérilisation de l'équipement. Si elle l'estime nécessaire, l'ACIA peut imposer des conditions supplémentaires à l'isolement des essais afin d'atténuer la propagation du produit nouveau.
9.16 Plan d'urgence
Tous les requérants doivent présenter un plan d'urgence visant à atténuer tout effet néfaste d'une dissémination accidentelle du produit. Cela comprend la description détaillée des méthodes de nettoyage et d'élimination en cas de déversement ou de rejet accidentel du produit, du matériel végétal traité ou des milieux de croissance contaminés par le supplément nouveau ou l'engrais contenant un supplément nouveau.
10. Inspection
Tous les essais à des fins de recherche menés au Canada sur les suppléments nouveaux et les engrais contenant un supplément nouveau peuvent être assujettis à une inspection par l'ACIA. L'ACIA produira un formulaire de rapport d'inspection détaillé visant à vérifier la conformité de l'essai à toutes les conditions prescrites par l'autorisation de recherche. Les inspecteurs de l'ACIA peuvent demander l'aide du chercheur ou du collaborateur de l'essai pour remplir toutes les informations sur le formulaire. La coopération des chercheurs est fort appréciée. Après l'inspection des champs, l'inspecteur enverra un rapport détaillé à la section de l'innocuité des engrais pour examen et suivi. Toute modification apportée au protocole de recherche doit être soumise pour examen à la section de l'innocuité des engrais et doit être approuvée par celle-ci avant l'inspection de l'essai.
11. Dossiers et communication de données
En plus de la surveillance par la collecte de données, les essais doivent être surveillés par le chercheur responsable sur une base régulière (fréquence minimale : une fois toutes les quatre semaines) dans le but d'évaluer la santé des végétaux, l'isolement de la culture à l'intérieur des parcelles du champ de l'essai, la santé des végétaux avoisinants, etc. Les parcelles de traitement devraient aussi être comparées aux parcelles de contrôle afin d'identifier tous les effets néfastes potentiels du supplément nouveau ou de l'engrais contenant un supplément nouveau. Les observations devraient être enregistrées en conséquence. L'ACIA ne fournit pas de modèles pour ces fiches d'observation.
Tout effet imprévu que l'on peut attribuer à la dissémination ou à la propagation du supplément nouveau ou de l'engrais contenant un supplément nouveau mis à l'essai doit être signalé à l'ACIA dès qu'il est observé. Si des effets néfastes associés à la dissémination du produit sont observés, l'ACIA peut annuler l'autorisation de recherche et exiger des mesures correctives pour atténuer les risques.
12. Coordonnées
Section de l'innocuité des engrais
Agence canadienne d' inspection des aliments
Téléphone : 1-855-212-7695
Adresse courriel : cfia.paso-bpdpm.acia@inspection.gc.ca
Annexe A : Exemples de cartes acceptables
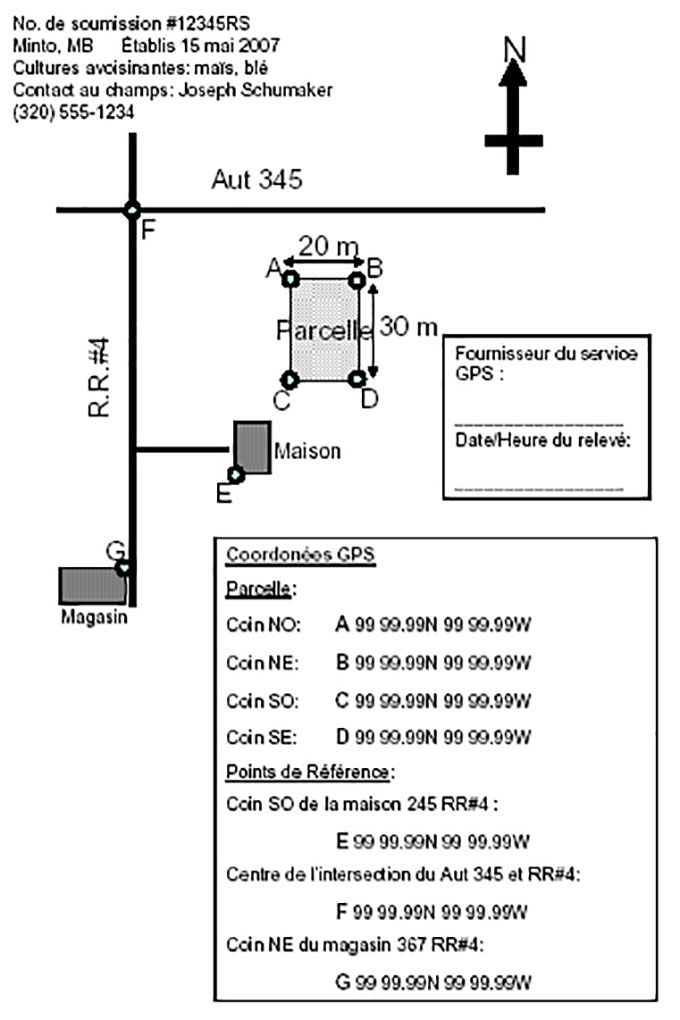
Description de l'image – Exemple 1 des cartes acceptables
Le texte suivant apparaît dans le coin supérieur gauche de l'image :
No. de soumission # 12345RS
Minto, MB Établis le 15 mai 2007
Cultures avoisinantes: maïs, blé
Contact au champ : Joseph Schumaker
320-555-1234
Dessous le texte il y a une carte.
Dans le haut, il y a une flèche pointant vers le haut avec un N montrant que le haut de la carte est le nord.
La carte montre deux lignes qui se coupent en haut à gauche de la carte. La ligne verticale représente le R.R. # 4 et la ligne horizontale représente l'autoroute 345.
Au bas de la route R.R. # 4 se trouve une case qui représente un magasin et est identifiée par la lettre G. Vers le haut de la ligne R.R. # 4 où la R.R. # 4 croise l'autoroute 345 il y a la lettre F. Vers le bas de la R.R. # 4, il y a une courte ligne et à la fin de la ligne il y a la lettre E qui représente une maison. Au-dessus de la maison, il y a un rectangle qui représente la parcelle qui est de 20 m×30 m et il y a une lettre (A, B, C, D) dans chaque coin. À droite de la maison, il y a une boîte qui contient le texte suivant :
Fournisseur du service GPS :
Date / Heure du relevé :
Au-dessous de la maison, il y a une boîte qui contient le texte suivant :
Coordonnées GPS
Parcelle
Coin NO : A 99 99.99N 99 99.99W
Coin NE : B 99 99.99N 99 99.99W
Coin SO : C 99 99.99N 99 99.99W
Coin SE : D 99 99.99N 99 99.99W
Points de référence
Coin SO de la maison 245 RR#4 :
E 99 99.99N 99 99.99W
Centre d'intersection du Aut 345 et RR#4 :
F 99 99.99N 99 99.99W
Coin NE du magasin 367 RR#4 :
G 99 99.99N 99 99.99W
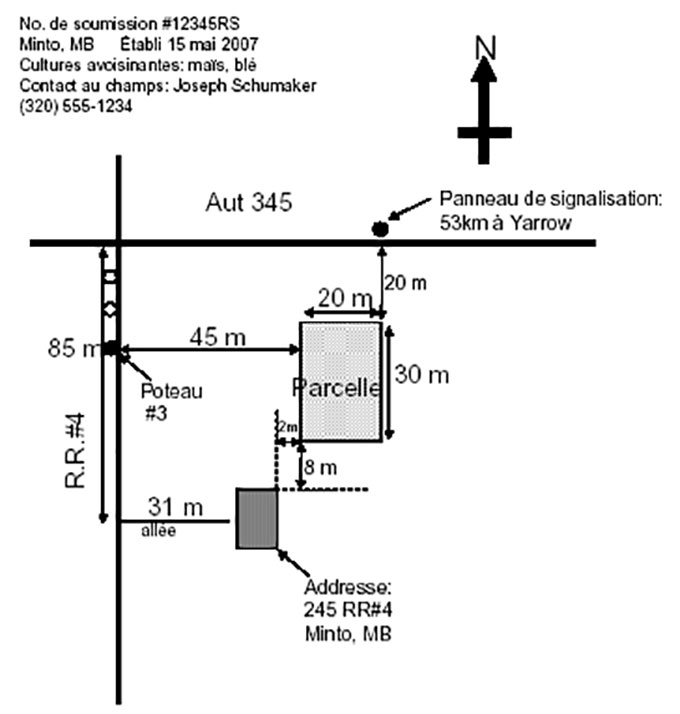
Description de l'image – Exemple 2 des cartes acceptables
Le texte suivant s'affiche dans le coin supérieur gauche de l'image:
No. de soumission # 12345RS
Minto, MB Établis le 15 mai 2007
Cultures avoisinantes: maïs, blé
Contact au champ : Joseph Schumaker
320-555-1234
Dessous le texte il y a une carte.
En haut, il y a une flèche pointant vers le haut avec un N montrant que le haut de la carte est le nord.
La carte montre deux lignes qui se coupent dans le coin supérieur gauche de la carte. La ligne verticale représente R.R. # 4 et la ligne horizontale représente l'autoroute 345.
À 20 m de l'Autoroute 345 sur la R.R. # 4, il y a un poteau # 3 et 45 m à droite de ce pôle, il y a une parcelle 20 m×30 m. 85 m de l'Autoroute 345 sur la R.R. # 4, il y a une allée de 31 m et à la fin de l'allée il y un rectangle dont l'adresse est 245 RR#4, Minto, MB