Janvier 2026
Sur cette page
- Abréviations
- Glossaire
- 1.0. Introduction
- 1.1. Objectif du guide
- 1.2. Aperçu réglementaire : Enregistrements en vertu de la Loi sur les engrais
- 1.3. Avant de commencer : déterminez si votre produit doit être enregistré
- 1.4. Procédures d'examen des dossiers et normes de prestation de services
- 1.5. Mon ACIA : plateforme de demande électronique
- 1.6. Format de la demande
- 1.7. Modification d'un produit enregistré
- 2.0. Structure et présentation de la demande
- 2.1. Demande d'autorisation Bureau de présentation des demandes préalables à la mise en marché (BPDPM)
- 2.2. Détails du produit I
- 2.3. Détails du produit II – Autres qualités et caractéristiques
- 2.4. Détails du produit II – Évaluation de l'innocuité
- 2.5. Nom et adresse du fabricant
- 2.6. Étiquette proposée pour le marché
- 3.0. Coordonnées
- Annexes
- Annexe 1 : Format de demande d'enregistrement d'un produit
- Annexe 2 : Exigences propres aux ingrédients pour démontrer leur innocuité
- Annexe 3 : Normes et seuils relatifs aux métaux, aux dioxines et aux composés de type dioxine et niveaux maximaux acceptables d'organismes indicateurs dans les engrais et les suppléments
- Annexe 4 : Caractérisation des dangers toxicologiques
- Annexe 5 : Évaluation de l'exposition et du risque toxicologique
- Annexe 6 : Caractérisation du danger microbien (liste de vérification)
- Annexe 7 : Caractérisation de l'exposition à un microorganisme – facteurs à considérer
- Annexe 8 : Considérations relatives à la classification de la gravité du danger microbien et du niveau d'exposition
- Annexe 9 : Exigences en matière d'étiquetage pour les engrais-pesticides autorisés pour un usage domestique ou de jardinage
- Annexe 10 : Ressources - Toxicologie
- Annexe 11 : Ressources – Microbiologie
Abréviations
- ACIA
- Agence canadienne d'inspection des aliments
- AQ
- Assurance qualité
- ARLA
- Agence de réglementation de la lutte antiparasitaire
- ATCC
- American Type Culture Collection
- BPC
- Biphényle polychloré
- BPDPM
- Bureau de présentation de demande préalables à la mise en marché
- BPL
- Bonne pratique de laboratoire
- CQ
- Contrôle de la qualité
- DL50/CL50
- Dose Létale médiane / Concentration Létale médiane
- DE50/CE50
- Dose Efficace médiane / Concentration Efficace médiane
- DI50/CI50
- Dose Infectieuse médiane / Concentration Infectieuse médiane
- DME(N)O
- Dose minimale avec effet (nocif) observé
- DSE(N)O
- Dose sans effet (nocif) observé
- EPA
- Environmental Protection Agency
- ET
- Équivalent toxique
- IQ
- Demande d'information sur un produit spécifique
- ISO
- Organisation internationale de normalisation
- LQ
- Limite de quantification
- No CAS
- Numéro du Chemical Abstracts Service
- NPP
- Nombre le plus probable
- NPS
- Normes de prestation de services
- NRD
- Numéro de référence de dimension
- PCDD
- Dioxines
- PCDF
- Furannes
- RA
- Résultats d'analyses
- RCC
- Renseignements commerciaux confidentiels
- SD
- Seuil de détection
- SIE
- Section de l'innocuité des engrais
- SIMDUT
- Système d'information sur les matières dangereuses utilisées au travail
- UFC
- Unité formant des colonies
Glossaire
- Assurance de la qualité (AQ)
- Approche systématique qui vise le maintien d'un niveau prédéterminé de la qualité d'un produit en portant attention à toutes les étapes de son processus de fabrication afin d'éviter toute insuffisance au moment de l'élaboration du produit.
- Composant actif
- Composant d'un engrais ou d'un supplément auquel un rendement en tant qu'engrais ou supplément est attribué.
- Contrôle qualité (CQ)
- Processus qui vise le maintien des normes relatives aux produits manufacturés, en analysant des échantillons du produit final pour vérifier leur conformité aux normes, afin de s'assurer de la qualité du produit final et de déceler toute anomalie après la fabrication et avant la mise en marché.
- Engrais
- Substance ou mélange de substances, contenant de l'azote, du phosphore, du potassium ainsi que tout autre élément nutritif des plantes, fabriqué ou vendu à ce titre ou représenté comme tel.
- Fiche de données de sécurité
- Bulletin technique exhaustif décrivant les dangers physico-chimiques, compositionnels, pour la santé humaine et environnementale, les premiers soins, les contrôles toxicologiques, écologiques, les précautions, les protections personnelles et les contrôles d'exposition, les renseignements sur la manipulation, l'entreposage, l'élimination, la lutte contre l'incendie, le déversement accidentel, la stabilité et la réactivité, les informations relatives au transport et à la réglementation d'une substance ou d'un produit.
- Infectivité
- Capacité d'un microorganisme de traverser ou d'éviter les barrières naturelles d'un hôte contre l'infection (la capacité d'un microorganisme d'envahir un organisme, de s'y maintenir à l'état viable ou de s'y multiplier, avec ou sans manifestation d'une maladie).
- Micro-organisme
- Bactérie, algue, champignon, protozoaire, virus, mycoplasme ou rickettsie et organismes apparentés.
- Pathogène
- Tout microorganisme qui peut provoquer une maladie.
- Pathogénicité
- Capacité d'un microorganisme d'infecter un hôte, de s'y établir et de s'y multiplier, puis d'infliger des lésions ou des dommages susceptibles ou non de mener à la mort.
- Substance
- Toute matière organique ou inorganique distincte, animée ou inanimée. Cette définition inclut une culture pure d'un micro-organisme. Un mélange de micro-organismes ou un produit microbien est un mélange de substances plutôt qu'une substance individuelle.
- Supplément
- Substance ou mélange de substances, autre qu'un engrais, fabriqué ou vendu pour enrichir les sols ou favoriser la croissance des plantes ou la productivité des récoltes, ou représenté comme pouvant servir à ces fins.
- Toxicité
- Capacité d'une substance à provoquer des effets néfastes sur les plantes ou les animaux vivants en raison de sa nature toxique.
- Toxigénicité
- Capacité d'un micro-organisme à produire une toxine.
- Toxine microbienne
- Substance produite par un micro-organisme qui est susceptible d'avoir un effet nocif sur un organisme hôte, indépendamment de la présence ou non du microorganisme vivant.
1.0. Introduction
1.1. Objectif du guide
Nous fournissons une gamme de ressources en ligne afin de mieux faire connaître et comprendre les exigences réglementaires relatives aux engrais et aux suppléments importés ou vendus au Canada. Le présent guide porte spécifiquement sur les exigences en matière d'information pour les produits assujettis à l'enregistrement.
Il vise à aider les demandeurs potentiels à préparer des demandes complètes et bien organisées, ce qui contribue à :
- simplifier le processus de révision des dossiers
- réduire les risques de retards ou de rejets
- accélérer la mise en marché
1.2. Aperçu réglementaire : Enregistrements en vertu de la Loi sur les engrais
Les engrais (éléments nutritifs essentiels pour les plantes) et les suppléments (produits autres que les engrais qui améliorent l'état physique du sol ou favorisent la croissance des plantes ou le rendement des cultures) importés ou vendus au Canada sont réglementés en vertu de la Loi sur les engrais et du Règlement sur les engrais, qui sont administrés par nous.
La Loi sur les engrais et son règlement d'application exigent que tous les produits réglementés soient sans danger pour la santé humaine, animale et végétale ainsi que pour l'environnement et qu'ils soient correctement étiquetés afin d'éviter toute fausse déclaration sur le marché.
Enregistrement
- La plupart des suppléments et certains engrais doivent faire l'objet d'une évaluation et d'un enregistrement obligatoires avant leur mise en marché au Canada
- Les enregistrements sont valides pour une période de 60 mois à partir de leur date d'émission
- Pour continuer à vendre ou à importer un produit enregistré au-delà de cette période, les demandeurs doivent nous présenter une demande de réenregistrement
Représentation véridique
Les produits doivent être présentés de manière précise et véridique sur le marché afin de protéger les consommateurs et de prévenir la fraude. Par exemple, si un produit répond à la définition d'un supplément, il doit être commercialisé en tant que tel. Il est inacceptable de supprimer des allégations ou des garanties, ou de présenter un produit de manière trompeuse afin d'éviter son enregistrement.
Surveillance de la conformité et application de la loi
Tous les produits réglementés en vertu de la Loi sur les engrais et de son règlement sont soumis à une surveillance du marché. Cela comprend l'inspection des produits, l'échantillonnage et des tests, ainsi que la vérification des étiquettes. Les produits jugés non conformes peuvent faire l'objet de mesures réglementaires, y compris la détention (interdiction de vente). En cas de non-conformité grave ou répétée, des poursuites peuvent être engagées.
1.3. Avant de commencer : déterminez si votre produit doit être enregistré
Avant de préparer une demande d'enregistrement, il est essentiel de confirmer si votre produit est soumis à l'enregistrement en vertu de la Loi sur les engrais. Tous les engrais et suppléments ne nécessitent pas d'enregistrement et la soumission d'une demande pour un produit exempté entraînera son rejet et le non-remboursement des frais.
Pour déterminer si votre produit doit être enregistré, consultez nos déclencheurs de l'enregistrement des engrais et des suppléments. Cette ressource comprend :
- définitions des engrais et des suppléments
- liste de matières et de types de produits exemptés
- organigrammes pour aider à évaluer les exigences d'enregistrement pour :
- produits à composant unique
- mélanges
- produits contenant des semences ou des milieux de culture
Si vous avez des doutes après avoir consulté la page sur les déclencheurs, vous pouvez nous soumettre une demande de renseignements (IQ) pour obtenir des conseils spécifiques à votre cas. Les demandes de renseignements sont gratuites et traitées dans un délai de 30 jours ouvrables.
Important
L'importation d'engrais et de suppléments peut être assujettie à des exigences réglementaires supplémentaires en vertu de la Loi sur la protection des végétaux et de la Loi sur la santé des animaux, selon la composition du produit.
- Les produits contenant de la terre ou des matières d'origine végétale peuvent être assujettis aux exigences de la Loi sur la protection des végétaux
- Les produits contenant des matières d'origine animale peuvent être assujettis aux exigences de la Loi sur la santé des animaux
Ces exigences s'appliquent, que le produit doive ou non être enregistré en vertu de la Loi sur les engrais.
Pour déterminer les exigences applicables en matière d'importation, les utilisateurs doivent consulter le Système automatisé de référence sur l'importation (SARI) avant l'importation. Des renseignements supplémentaires sont disponibles sur notre site Web (Plantes ou Animaux).
1.4. Procédures d'examen des dossiers et normes de prestation de services
Les procédures et les délais d'examen des demandes d'enregistrement (nouveaux enregistrements, réenregistrements, modifications majeures et mineures) sont décrits dans la circulaire à la profession T-4-122 : Normes de prestation de services s'appliquant aux demandes d'enregistrement des engrais et suppléments.
Les normes de prestation de services (NPS) comprennent à la fois le délai d'examen par l'ACIA et le temps dans la file d'attente, car toutes les demandes sont traitées dans l'ordre où elles sont reçues. Les délais varient en fonction du type de demande, reflétant la complexité de l'évaluation requise. Chaque demande peut faire l'objet d'un maximum de 3 cycles d'évaluation, bien que tous les examens ne soient pas obligatoires. Si aucune lacune n'est constatée au cours d'une évaluation donnée, un produit peut être enregistré (ou une modification accordée) à l'issue de cette étape d'évaluation.
Afin d'éviter tout retard, il est essentiel que les demandeurs comprennent parfaitement les exigences d'enregistrement avant de nous présenter leur demande.
Réponse aux lacunes
Si des lacunes sont identifiées au cours du premier cycle d'évaluation, les demandeurs doivent répondre à chacune de nos questions posées en fournissant des informations complètes et détaillées. Les réponses incomplètes ou soumises après la date limite spécifiée sont considérées comme non conformes et le dossier sera fermé. Il est fortement recommandé d'inclure une lettre d'accompagnement dans la demande initiale et en réponse à chaque étape d'évaluation.
De plus, un dossier sera fermé si le demandeur présente de nouvelles informations au cours du processus d'évaluation, telles que des modifications substantielles de la composition ou du procédé de fabrication du produit, qui nécessiteraient une évaluation différente ou plus approfondie.
1.5. Mon ACIA : plateforme de demande électronique
Nous offrons des services numériques par l'intermédiaire de notre plateforme en ligne sécurisée Mon ACIA. Cette plateforme permet aux utilisateurs de demander des services, d'effectuer des paiements et de suivre l'état d'avancement des demandes en ligne. Les comptes peuvent être personnalisés en fonction des différents modèles commerciaux et des besoins opérationnels.
Grâce à Mon ACIA, les demandeurs peuvent soumettre des demandes de service au BPDPM pour toute une série de demandes liées aux engrais et aux suppléments, notamment :
- nouveaux enregistrements
- renouvellements d'enregistrement
- modifications majeures et mineures
- enregistrements de marques privées
- autorisations de recherche
Pour aider les utilisateurs, nous proposons diverses ressources, notamment des documents d'orientation, des vidéos explicatives et des guides étape par étape. Ces documents expliquent comment créer et gérer un compte et comment soumettre des demandes de service en ligne. Pour plus d'informations, consultez : Mon ACIA – Orientation de l'utilisateur
1.6. Format de la demande
Chaque demande comprend les 5 sections suivantes :
- Formulaires administratifs et frais
- Détails du produit I
- Détails du produit II – Autres qualités et caractéristiques
- Détails du produit II – Évaluation de la sécurité
- Étiquette commerciale
(Veuillez noter que celles-ci étaient auparavant appelées « onglets » ; voir l'annexe 1)
Le système de soumission invite les utilisateurs à saisir des informations à l'aide de champs à remplir et de téléchargements de documents.
Les fichiers téléchargés doivent être clairement nommés afin de refléter leur contenu.
Exemple : Détail_du_produit_II_Procédé_de_fabrication.pdf
Les utilisateurs ne peuvent passer à la section suivante tant que tous les champs obligatoires n'ont pas été remplis.
Exigences générales relatives à la soumission
- N'omettez pas les détails obligatoires sur le produit et ne sautez pas les message de téléchargement.
Si une section ne s'applique pas, veuillez inclure une brève explication écrite.
Exemple : « Ce produit est proposé comme présentant un niveau de risque II pour la sécurité. À ce titre, aucune justification en matière de sécurité n'a été soumise. » - Les demandes peuvent faire référence à des soumissions antérieures par leur numéro, mais chaque demande doit être complète et indépendante. Les évaluateurs de l'ACIA ne récupéreront pas les informations contenues dans les demandes antérieures. Cela s'applique aux demandes de renouvellement, aux modifications et aux demandes de marques privées (anciennement appelées « demandes me-too »). Toutes les demandes doivent inclure l'ensemble complet des informations requises.
- Les demandes incomplètes seront rejetées
Ressources utiles : Listes de contrôle des demandes
Afin d'aider les demandeurs à préparer un dossier d'enregistrement complet et conforme, nous fournissons des listes de contrôle détaillées pour les engrais et les suppléments. Ces listes de contrôle décrivent les documents et les informations justificatives requis pour chaque type de demande. Consultez la présentation générale de l'enregistrement des engrais de l'ACIA et les listes de contrôle des demandes pour obtenir des conseils étape par étape.
1.7. Modification d'un produit enregistré
Modifications et amendements apportés aux produits
Aucune modification ne peut être apportée à l'étiquette, à la composition chimique ou aux ingrédients d'un produit si cette modification est susceptible d'affecter l'identité du produit en tant qu'engrais ou supplément, son innocuité ou son utilisation prévue, à moins que l'enregistrement ne soit modifié en conséquence (par une modification majeure ou mineure) ou que la modification ne soit apportée lors d'un réenregistrement.
Les modifications qui n'ont aucune incidence sur l'identité, l'innocuité ou l'utilisation du produit peuvent être apportées sans notre accord préalable et ne nécessitent aucune notification. Contactez-nous si vous avez des questions pour savoir si les modifications que vous envisagez d'apporter à votre ou vos produits nécessitent la soumission d'une modification.
Demande de renseignements sur le changement de source d'un ingrédient (ISCI)
Si un demandeur souhaite modifier la source d'un ingrédient (et non l'ingrédient lui-même) et qu'il n'est pas certain que cette modification ait une incidence sur l'innocuité du produit, il peut nous soumettre une demande (section 4.5 de la circulaire T-4-122). La demande doit décrire la modification proposée et demander des conseils sur la nécessité ou non de modifier l'enregistrement. Les demandes sont gratuites et traitées dans un délai de 30 jour ouvrable.
Résultats possibles:
- approbation : si la nouvelle source ne pose aucun problème d'innocuité, elle sera approuvée sans examen supplémentaire
- modification majeure requise : si la modification est susceptible d'avoir une incidence sur l'innocuité ou l'identité du produit (p. ex. passage d'une source minière à une source recyclée potentiellement contaminée), une demande de modification complète sera requise avant le changement
2.0. Structure et présentation de la demande
2.1. Demande d'autorisation Bureau de présentation des demandes préalables à la mise en marché (BPDPM)
Cette section décrit les exigences administratives relatives à la présentation d'une demande d'enregistrement d'engrais ou de supplément.
2.1.1 - Lettre d'accompagnement
La lettre d'accompagnement est un outil de communication important qui aide notre personnel à comprendre le contexte et l'intention de votre demande. Une lettre d'accompagnement claire et bien structurée facilite la classification précise et le traitement efficace des dossiers pendant le processus de présélection et d'examen.
Les demandeurs doivent inclure les informations suivantes dans la lettre d'accompagnement :
- Type de demande par exemple :
- nouvel enregistrement
- réenregistrement
- modification majeure
- modification mineure
- Niveau d'évaluation de l'innocuité (niveau I, II ou III)
Remarque : Nous validerons cette catégorisation lors de l'examen initial et pourront la modifier si nécessaire. - Numéros de référence, y compris les numéros de contrôle de la demande (p. ex. pour une demande de renseignements : 12345IQ) et tout numéro d'enregistrement accordé antérieurement et pertinent pour la demande actuelle
- Utilisation finale prévue du produit par exemple :
- agriculture
- serre
- gazon
- pelouse résidentielle
- maison – intérieur
- inoculation de semences
- mélange
Important
Il n'y a pas de champ de téléchargement dédié à la lettre d'accompagnement dans Mon ACIA. Les demandeurs peuvent joindre la lettre d'accompagnement en utilisant n'importe quel champ de téléchargement disponible et s'assurer qu'elle est clairement nommée (p. ex. Lettre_d'acompagnement.pdf) afin qu'elle puisse être facilement identifiée par notre personnel.
2.1.2 - Représentant autorisé et agent canadien
Avant de procéder à l'enregistrement d'un produit, il est nécessaire d'identifier une personne autorisée à représenter le demandeur/représentant canadien et avec laquelle l'Agence pourra correspondre au sujet de la demande.
Nous ne divulguerons aucune information concernant la demande et ne discutera pas de son statut avec toute personne qui n'est pas un représentant autorisé, un contact du profil ou le demandeur.
Il n'est pas obligatoire que le déclarant/demandeur réside au Canada. Toutefois, pour les demandeurs résidant à l'extérieur du Canada, un agent canadien résident doit également être désigné en remplissant les champs nom et adresse dans Mon ACIA. L'agent canadien peut recevoir toute notification légale ou correspondance, le cas échéant. Un agent canadien doit être une personne physique et non une société et cette personne doit être un résident permanent du Canada.
Le fait d'être désigné comme agent canadien ne signifie pas automatiquement que la personne est un représentant autorisé. L'agent canadien ne recevra des courriels et des notifications automatiques que si cette personne est également un représentant autorisé, un contact du profil ou le demandeur.
2.1.3 - Frais d'enregistrement
Pour initier l'évaluation d'un dossier, les demandeurs doivent payer les frais d'enregistrement applicables, tels qu'indiqués dans la partie 5 de notre avis sur les frais.
Les frais s'appliquent aux demandes présentées en vertu de la Loi sur les engrais aux fins suivantes :
- nouvel enregistrement
- renouvellement
- modification d'un enregistrement existant (majeure ou mineure)
- évaluation de l'innocuité d'un produit
Demandes d'évaluation de l'innocuité uniquement
Si le demandeur sollicite uniquement une évaluation de l'innocuité (c'est-à-dire qu'il ne demande pas d'enregistrement), les frais d'enregistrement ne s'appliquent pas. Ces demandes sont classées dans la catégorie « Données sur l'innocuité » (DS) et seuls les frais d'évaluation de l'innocuité sont payables au moment de la soumission.
Niveaux d'évaluation de l'innocuité
Afin d'assurer la cohérence pour les parties réglementées, les frais d'évaluation de l'innocuité s'appliquent à toutes les évaluations d'innocuité de niveau II et III (voir la section 2.4.1 pour les définitions) telles que définies dans le présent guide.
| Type de produit | Frais d'enregistrement | Frais d'évaluation de l'innocuité |
|---|---|---|
| Modification majeure (AM) | cocher | Note de tableau a |
| Modification mineure (MA) | cocher | - |
| Nouvel enregistrement (NR) Niveau I | cocher | - |
| Nouvel enregistrement (NR) Niveau II | cocher | cocher |
| Nouvel enregistrement (NR) Niveau III | cocher | cocher |
| Nouvel enregistrement (NR) Marque privée | cocher | - |
| Réenregistrement (RR) | cocher | Note de tableau a |
2.2. Détails du produit I
Cette section recueille les informations clés permettant d'identifier le produit. Les détails saisis doivent correspondre exactement à ceux qui figurent sur l'étiquette du produit ou dans le texte de l'étiquette joint à la demande.
2.2.1 - Confirmer les détails du produit
Type de produit (obligatoire)
Sélectionnez le type de produit approprié dans le menu déroulant.
Les définitions suivantes vous aideront à choisir la catégorie appropriée :
- 1. Engrais commercial
- Toute substance ou mélange de substances contenant de l'azote, du phosphore, du potassium ou d'autres nutriments végétaux, fabriqué, vendu ou présenté pour être utilisé comme nutriment végétal.
- 2. Engrais -antiparasitaire
- Produit combiné qui comprend des allégations relatives à la résistance aux pesticides ou aux maladies. Si le pesticide n'est pas homologué en vertu de la Loi sur les produits antiparasitaires pour l'utilisation et le taux d'application allégués, l'approbation et/ou l'homologation de l'Agence de réglementation de la lutte antiparasitaire (ARLA) est requise.
- 3. Engrais domestique et jardinage
- Engrais recommandés pour une utilisation exclusive sur les plantes d'intérieur et dans les jardins urbains.
- 4. Engrais hydroponiques (sans sol)
- Engrais destinés à être utilisés dans des systèmes hors sol. Tels que la culture hydroponique.
- 5. Oligo-éléments
-
Engrais contenant 1ou plusieurs des oligo-éléments suivants :
- bore (B)
- chlore (Cl)
- cuivre (Cu)
- fer (Fe)
- molybdène (Mo)
- manganèse (Mn)
- zinc (Zn)
- 6. Supplément
-
Substance ou mélange de substances, autre qu'un engrais, fabriqué ou vendu pour enrichir les sols ou favoriser la croissance des plantes ou la productivité des récoltes, ou représenté comme pouvant servir à ces fins. Les effets conférés par le produit peuvent être directs ou indirects.
Les suppléments enregistrables peuvent être de nature chimique (par exemple, régulateurs de croissance des plantes, agents mouillants) ou microbienne (contenant des micro-organismes viables).
Il convient de noter que lorsqu'un supplément est inclus dans un engrais, le type de produit est attribué en fonction du type d'engrais.
- 7. Marque privée
- Réservé aux cas où un demandeur souhaite enregistrer un engrais ou un supplément déjà enregistré sous un autre nom et/ou une autre marque. Pour plus d'informations, consultez la ciculaire T-4-122.
Marque de commerce (optionel)
Entrez le nom de marque exactement tel qu'il apparaît sur l'étiquette du produit commercialisé.
La marque désigne toute marque distinctive ou tout nom commercial, autre que le nom et la catégorie exigés par le Règlement sur les engrais, qui est appliqué par le fabricant, le titulaire de l'enregistrement ou le vendeur afin de distinguer l'engrais ou le supplément de tout autre produit.
Remarque : Si le nom de marque diffère en français et en anglais, inscrivez les deux versions.
Nom du produit et/ou catégorie (obligatoire)
Entrez le nom du produit exactement tel qu'il apparaît sur l'étiquette du marché. Si le nom est identique en anglais et en français, entrez-le de manière identique dans les deux champs.
Le cas échéant, le nom du produit doit contenir :
- la catégorie : quantité totale d'azote, d'acide phosphorique disponible et de potasse soluble dans un engrais, exprimée en pourcentage sous forme N-P-K. Les valeurs peuvent être des nombres entiers ou des décimales.
- le pourcentage et le nom de l'ingrédient actif pesticide garanti.
Pour plus d'informations sur le nom et l'identité du produit, veuillez consulter la section 2.6 Étiquette commerciale proposée
Important : Nous nous réservons le droit de refuser une demande si les renseignements fournis sont incomplets.
2.2.2 - Substances constituantes
Tous les ingrédients du produit, actifs et inertes, doivent être clairement identifiés et énumérés dans cette section. Les renseignements soumis sont destinés uniquement aux évaluateurs de l'ACIA et sont traités comme des renseignements commerciaux confidentiels (RCC). Ils sont protégés en vertu des lois sur l'accès à l'information et la protection des renseignements personnels et ne seront pas divulgués sans le consentement écrit du titulaire de l'enregistrement.
Si le demandeur de l'enregistrement n'est pas en mesure d'obtenir les détails relatifs aux ingrédients exclusifs, le distributeur ou le fabricant peut les soumettre directement au BPDPM , à l'adresse cfia.paso-bpdpm.acia@inspection.gc.ca. Ces soumissions seront signalées comme étant la propriété d'un tiers et resteront confidentielles.
Si votre réponse aux exigences d'examen du dossier comprend des RCC de tiers, veuillez l'indiquer clairement dans votre réponse. Ne marquez la tâche comme complète dans Mon ACIA qu'après avoir reçu la confirmation que le tiers nous a soumis les informations requises.
2.2.2.1 - Ingrédients
Pour toutes les matières utilisées dans la production d'un engrais ou d'un supplément enregistrable (à l'exception des inoculums microbiens décrits à la section (2.2.2.2)) les informations suivantes sont requises :
- nom de la matière
- numéro CAS (Chemical Abstracts Service), s'il est disponible
- fabricant
- pays d'origine
- type de source (par exemple, fabriqué, récolté, extrait, sous-produit, matières organiques recyclées Note de bas de page 1, synthétisé Note de bas de page 2)
- procédés de fabrication/purification de l'ingrédient, le cas échéant
- concentration du matériau dans le produit final (les entrées doivent totaliser 100 %)
- l'utilité de l'ingrédient dans la formulation ; et
- fiches de données de sécurité
Remarque : Plusieurs sources pour un ingrédient peuvent être identifiées au moment de l'enregistrement du produit et utilisées de manière interchangeable. Toutefois, toute modification apportée aux ingrédients, aux sources, aux fournisseurs ou à la formulation après l'enregistrement nécessite une modification majeure, sauf si nous avons approuvé un changement de source d'ingrédient (voir la section 4.5 de la circulaire T-4-122 pour plus d'informations sur les demandes de changement de source d'ingrédient).
Veuillez consulter le tableau 2 ci-dessous pour connaître la méthode privilégiée pour soumettre les données requises.
| Substances constituantes | Numéro d'enregistrement, le cas échéant | Numéro CAS (Chemical Abstract Service), le cas échéant | Fabricant/fournisseur | Pays d'origine | Source et brève description de la méthode de fabrication | Proportion | Concentration dans le produit final | Utilité du matériau |
|---|---|---|---|---|---|---|---|---|
| - | - | - | - | - | - | - | Total: 100 % | - |
2.2.2.2 - Inoculums microbiens
Pour les produits contenant des micro-organismes viables d'origine naturelle, les informations suivantes sont requises :
- utilité de la souche microbienne
- identification taxonomique au niveau du genre et de l'espèce ; sous-espèce et souche (si disponible)
- résultats analytiques appuyant la classification taxonomique (y compris les données brutes)
- relation avec des agents pathogènes connus (par exemple, arbres phylogénétiques ou alignements comparatifs de séquences)
- origine du micro-organisme (source et lieu d'isolement) ou numéro d'accès à la banque de souches et certificat de culture provenant d'une collection de cultures reconnue (par exemple, l'American Type Culture Collection (ATCC)).
Exigences en matière d'identification
Une identification taxonomique solide et défendable, de préférence au niveau de la souche, est essentielle pour la caractérisation des dangers. Nous recommandons une approche polyphasique, combinant :
- analyse phénotypique (p. ex. morphologie, caractéristiques biochimiques)
- outils moléculaires par exemple :
- méthodes basées sur l'ADN
- l'ARN
- les protéines
Les méthodes doivent se compléter mutuellement afin de garantir une identification précise et une différenciation claire des espèces pathogènes ou toxigéniques.
Consortiums microbiens
Pour les consortiums microbiens (définis comme des communautés microbiennes complexes issues d'un seul environnement naturel et maintenues sans autre manipulation), fournir :
- description de l'environnement d'origine (par exemple, consortium associé au sol ou à la rhizosphère)
- détails du traitement confirmant que la composition d'origine est maintenue sans manipulation supplémentaire
Dans la mesure du possible, toutes les espèces individuelles doivent être identifiées. Si une identification précise n'est pas possible, une classification au niveau du genre ou de la famille peut être utilisée. Lorsque des regroupements taxonomiques sont fournis, le consortium doit être soumis à un dépistage des espèces dangereuses pertinentes pour le type de produit envisagé.
Les demandeurs doivent sélectionner des indicateurs appropriés en fonction du type de produit et de la source. Par exemple, le dépistage peut inclure des espèces pathogènes pour l'humain telles que :
- Salmonella spp.
- Listeria monocytogenes
- Vibrio spp.
- Campylobacter spp.
- Clostridium spp.
- Bacillus anthracis
- Pseudomonas aeruginosa
- Yersinia spp.
- Candida albicans
- Aspergillus fumigatus
- Faecal coliforms
- Enterococci
- Rotavirus
- Norovirus
- Ascaris lumbricoides
Veuillez noter que la section de l'innocuité des engrais peut demander des tests de dépistage supplémentaires pendant le processus d'évaluation. Les tests de pathogénicité doivent être effectués sur la formulation finale du produit.
Pour plus d'informations, veuillez consulter T-4-126 – Identification et classification taxonomique des micro-organismes présentés pour usage comme suppléments en vertu de la Loi sur les engrais.
Exigences en matière d'information pour les micro-organismes modifiés par des techniques de biologie moléculaire
Pour les micro-organismes qui ont été génétiquement modifiés à l'aide de techniques de biologie moléculaire, les informations suivantes doivent être fournies :
1. Aperçu de la modification génétique
- Schéma illustrant le processus de modification génétique, comprenant :
- carte de la construction insérée
- site d'insertion (chromosomique ou plasmidique)
- nombre de copies
- vecteur(s) de clonage utilisé(s)
- séquences du promoteur
- gènes marqueurs sélectionnables, y compris tout gène de résistance aux antibiotiques
- pour les techniques d'édition du génome (par exemple, CRISPR/Cas9 – Clustered Regularly Interspaced Short Palindromic Repeats/CRISPR-associated protein 9), fournir :
- description du mécanisme d'édition
- site(s) cible(s) et modifications prévues
- résultats des évaluations des effets non ciblés
- confirmation de la présence ou non d'ADN étranger dans le produit final
2. Caractérisation génétique et fonctionnelle
- Description détaillée du ou des produits géniques, y compris leurs propriétés et leurs fonctions prévues
- Identification de toute modification des voies métaboliques résultant de l'insertion génétique
- Évaluation des effets indésirables sur l'expression génétique (par exemple, régulation à la hausse ou à la baisse d'autres gènes)
- Évaluation de la stabilité du matériel génétique inséré
3. Considérations environnementales et d'innocuité
- Potentiel de transfert génétique horizontal, y compris :
- mécanismes de transfert (transformation, transduction, conjugaison)
- éléments génétiques mobiles impliqués par exemple :
- plasmides
- bactériophages
- éléments conjugatifs intégratifs
- transposons
- séquences d'insertion
- intégrons
- cassettes génétiques
- îlots génomiques
- Procédures et tests utilisés pour détecter et quantifier les micro-organismes modifiés
- Pour les endophytes, évaluation de la présence potentielle dans la partie comestible de la culture
4. Pureté de l'inoculum
Les demandeurs doivent fournir des preuves de la pureté de l'inoculum, notamment les éléments suivants :
Contrôle de la qualité de l'inoculum primaire
- Description des paramètres de contrôle de la qualité utilisés pour surveiller, identifier et purifier le micro-organisme à partir de l'inoculum primaire)
- Nom et adresse de l'entreprise qui conserve l'inoculum primaire
Contrôle de la qualité de l'inoculum final
- Description du processus de fabrication
- Paramètres de contrôle de la qualité utilisés pour surveiller l'identité et la pureté de l'inoculum final (généralement mélangé à des ingrédients inertes)
2.2.2.3 - Composition du produit final
L'identité et les proportions relatives en pourcentage poids/poids (totalisant 100 %) doivent être fournies pour tous les ingrédients présents dans le produit final, y compris :
- tous les ingrédients actifs et inertes
- les contaminants
- les résidus
- les sous-produits de réaction et produits de dégradation
Les ingrédients utilisés dans la fabrication du produit peuvent être les mêmes que les ingrédients présents dans le produit final s'il n'y a pas de réaction chimique ou de sous-produits métaboliques générés pendant la fabrication et l'entreposage du produit fini avant la vente et si aucune croissance de nouveaux microorganismes ne survient.
La fiche de données de sécurité du produit final doit être fournie avec la demande, si elle est disponible.
2.3. Détails du produit II – Autres qualités et caractéristiques
2.3.1 - Caractéristiques physiques du produit final
Par exemple :
- granulaire
- liquide
- pH
- couleur
- odeur
- numéro de référence de dimension (NRD)
2.3.2 - Méthode de fabrication
Les demandeurs doivent fournir une description détaillée du processus de fabrication du produit final, accompagnée d'un organigramme résumant chaque étape. Cette vue d'ensemble sert à évaluer le potentiel de réactions secondaires, de formation de sous-produits et/ou de contamination microbienne.
La description doit inclure :
- chaque étape du processus de production, dans l'ordre séquentiel
- le point auquel chaque ingrédient est incorporée, y compris sa proportion en poids
- les conditions de traitement associées à chaque étape, telles que :
- température
- pression
- durée
- type d'équipement de transformation utilisé
2.3.3 - Procédures d'assurance qualité et de contrôle de la qualité (AQ/CQ)
Afin de démontrer l'uniformité de la production et l'innocuité du produit final, les demandeurs sont tenus de fournir les informations suivantes concernant les procédures d'assurance qualité (AQ) et de contrôle de la qualité (CQ) utilisées pendant le processus de fabrication :
- justification de la conformité des matières premières aux spécifications et aux normes (accompagnée des analyses ou des accréditations, le cas échéant)
- le type de matières analysées (par exemple matières brutes, matières intermédiaires ou produit final)
- les caractéristiques des analyses et la sensibilité des méthodes d'analyse (limites de détection et/ou limites de quantification)
- identification des critères de « passage »
- fréquence des analyses (par exemple, par lot ou par unité de temps) et des points d'échantillonnage pendant la production
- surveillance des conditions de fabrication (par exemple, le temps, la pression, la teneur en humidité); et
- sort des lots non conformes (par exemple, retraitement, élimination)
2.3.4 - Analyse garantie
Les demandeurs doivent fournir le pourcentage minimum ou réel garanti de chaque nutriment pour les plantes ou autre ingrédient actif :
- les éléments nutritifs principaux (c-à-d , N, P, K) et secondaires (c-à-d , Ca, Mg, S) doivent être garantis sur une base minimale.
- les oligo-éléments (c-à-d, B, Cl, Cu, Fe, Mn, Mo, Zn) doivent être garantis sur une base réelle.
Pour obtenir des informations sur les garanties relatives aux autres ingrédients actifs, consultez la circulaire T-4-130 : Exigences en matière d'étiquetage des engrais et des suppléments.
Remarque : seules les garanties qui figurent sur l'étiquette commerciale doivent être incluses dans cette section.
Tous les ingrédients actifs doivent être garantis et les valeurs doivent correspondre à celles figurant sur l'étiquette commerciale.
Pour éviter toute représentation trompeuse :
- les déclarations d'origine et les listes d'ingrédients ne sont pas requises sur les étiquettes des produits enregistrés, car ceux-ci n'ont pas besoin de démontrer leur statut d'exemption.
- si une déclaration d'origine figure sur l'étiquette, elle doit être complète (inclure tous les intrants actifs) et être clairement séparée de la section « Analyse garantie » à l'aide d'une délimitation visuelle (par exemple, un espacement, une ligne ou une bordure).
2.4. Détails du produit II - Évaluation de l'innocuité
2.4.1 - Niveau d'évaluation de l'innocuité proposé (I, II ou III) et documents justificatifs
Afin de réduire la charge pour les parties prenantes et de faciliter l'enregistrement en vertu de la Loi sur les engrais et de son règlement d'application, nous utilisons une approche d'évaluation de l'innocuité à plusieurs niveaux. L'étendue des données d'innocuité requises dépend du type de produit, de sa composition et de son profil de risque.
- Toutes les demandes doivent inclure les informations essentielles sur le produit (niveau d'évaluation de l'innocuité I).
- Certaines demandes nécessitent des données analytiques (niveau d'évaluation de l'innocuité II) afin de vérifier l'uniformité de la production, l'efficacité du traitement et la pureté en ce qui concerne les niveaux de contaminants.
- Les produits à risque élevé ou à risque inconnu nécessitent une évaluation complète de l'innocuité (niveau d'évaluation de l'innocuité III), comprenant des justifications scientifiques, des données supplémentaires sur l'innocuité et/ou des résultats analytiques supplémentaires.
Le niveau d'évaluation de l'innocuité approprié (I, II ou III) est déterminé en fonction :
- les ingrédients du produit (actifs et inertes) et leurs sources
- les résidus, contaminants et sous-produits de dégradation potentiels
- méthode de fabrication
- le mode d'utilisation, le taux d'application et la fréquence
Reportez-vous au tableau 3 pour connaître les exigences en matière d'information pour chaque niveau d'évaluation de la sécurité.
| Niveau d'évaluation de l'innocuité | Exigences administratives | Détails du produit I | Détails du produit II | Étiquette commerciale | ||
|---|---|---|---|---|---|---|
| Représentant autorisé, lettre d'accompagnement ( Note de tableau aOnglet 1) |
Substances constituantes ( Note de tableau aOnglet 3) |
Autres qualités et caractéristiques - Méthode de fabrication, AQ/CQ ( Note de tableau aOnglet 3) |
Évaluation de l'innocuité - Résultats d'analyse ( Note de tableau aOnglet 4) |
Évaluation l'innocuité - Justification de l'innocuité ( Note de tableau aOnglet 5) |
( Note de tableau aOnglet 2) | |
| I | cocher | cocher | cocher | - | - | cocher |
| II | cocher | cocher | cocher | cocher | - | cocher |
| III | cocher | cocher | cocher | cocher Note de tableau b | cocher | cocher |
Un résumé des informations requises pour divers ingrédients figure à l'annexe 2.
Remarques supplémentaires
- Nous nous réservons le droit de demander des données supplémentaires sur l'innocuité, des justifications ou des analyses pour tout produit réglementé en vertu de la Loi sur les engrais, si des préoccupations en matière d'innocuité surgissent pendant l'examen de la demande.
- Les demandeurs sont encouragés à utiliser le processus demande d'information sur un produit spécifique (IQ) spécifique au produit pour clarifier les exigences en matière d'information avant de soumettre une demande.
- Si, après le processus de demande d'information, des questions subsistent, une consultation préalable à la présentation peut être demandée afin d'obtenir des conseils en matière de réglementation. Pour plus de détails, consultez Lignes directrices concernant les consultations préparatoires à une demande d'enregistrement pour les engrais et suppléments réglementés en vertu de la Loi sur les engrais et son règlement d'application.
2.4.2 - Résultats d'analyses
Les résultats d'analyse requis à l'appui d'une demande d'enregistrement varient selon le type de produit et la source des ingrédients. Des exemples de résultats d'analyse spécifiques aux ingrédients qui doivent être inclus dans une demande sont fournis à l'annexe 2.
Décrites à l'annexe 3 sont les normes d'innocuité et les limites utilisées par l'ACIA pour évaluer l'innocuité des produits et l'efficacité du traitement ou de la transformation en ce qui concerne
- les métaux
- les dioxines et les composés de type dioxine
- les organismes indicateurs
Cette annexe comprend également les tolérances maximales pour les garanties relatives à la teneur en oligo-éléments des engrais.
Guide de soumission des échantillons et des analyses de laboratoire
Les échantillons de produits doivent être prélevés à des intervalles permettant d'évaluer l'uniformité de la production. Voici quelques exemples :
- à intervalles réguliers
- à la réception des matières premières
- par lot ou par série
Les demandeurs doivent indiquer le nombre de lots produits chaque année.
Tous les résultats d'analyse que nous exigeons doivent répondre aux critères suivants :
- pmprimés sur papier à en-tête du laboratoire
- signés par l'analyste
- inclure :
- l'identification de l'échantillon
- méthode(s) de préparation de l'échantillon
- méthode(s) d'essai utilisée(s), y compris les seuils de détection (SD) et/ou les limites de quantification (LQ)
- identification de l'organisme de certification ou d'accréditation du laboratoire
2.4.2.1 - Exigences en matière d'analyse des métaux
Pour démontrer leur conformité à nos normes relatives aux métaux, les demandeurs doivent soumettre les résultats d'analyse des 11 métaux préoccupants suivants :
- arsenic (As)
- cadmium (Cd)
- cobalt (Co)
- cuivre (Cu)
- chrome (Cr)
- mercure (Hg)
- molybdène (Mo)
- nickel (Ni)
- plomb (Pb)
- sélénium (Se)
- zinc (Zn)
Nombre d'analyses requises
Le nombre d'analyses requises pour les métaux dépend du nombre total de lots produits au cours des 5 années précédant la demande (pour les nouveaux enregistrements ou les réenregistrements). Les exigences en matière d'échantillonnage sont présentées dans le tableau 4 ci-dessous.
Les analyses doivent refléter la production réelle sur la période de 5 ans. Par exemple, si 5 analyses sont requises, il est recommandé de soumettre 1 analyse pour chaque année civile.
Pour les produits fabriqués selon des procédés en continus, 6 séries d'analyses doivent être soumises, réparties de manière égale sur la période de 5 ans. Si le produit n'est pas encore fabriqué et que les résultats ne sont pas disponibles, veuillez contacter la Section de l'innocuité des engrais pour obtenir des conseils. Ces cas seront évalués individuellement.
| Nombre de lots fabriqués au cours des cinq années précédant la présentation de la demande | Nombre d'échantillons d'analyses requis |
|---|---|
| 1 | 1 |
| 2 à 4 | 2 |
| 5 à 9 | 3 |
| 10 à 16 | 4 |
| 17 à 25 | 5 |
| 26+ | Le requérant doit proposer un calendrier que nous devons approuver |
2.4.2.2 - Exigences en matière d'analyse pour les dioxines et composés de type dioxine
Pour démontrer leur conformité aux normes de l'ACIA relatives aux dioxines et aux composés de type dioxine, les demandeurs doivent soumettre 1 ensemble d'analyses des équivalents toxiques (TEQ) des dioxines et furanes (voir les tableaux 7 et 8, à l'annexe 3).
Remarque : la soumission d'analyses des dioxines et des composés de type dioxine n'est pas requise pour tous les produits.
2.4.2.3 - Exigences relatives à l'analyse des organismes indicateurs
Nous utilisons Salmonella et les coliformes fécaux comme organismes indicateurs pour évaluer la contamination par des agents pathogènes et l'efficacité du processus de traitement.
Pour démontrer leur conformité, les demandeurs doivent soumettre 4 séries de résultats d'analyse provenant de 4 lots distincts du produit final, testés à la fois pour les coliformes fécaux et Salmonella.
Dans le cas d'une production continue ou semi-continue, les échantillons doivent être prélevés à des intervalles d'au moins 2 semaines. Dans le cas d'une production par lots, les intervalles d'échantillonnage doivent refléter le calendrier de fabrication réel (voir le tableau 9, à l'annexe 3).
2.4.2.4 - Tolérances supérieures des garanties nutritionnelles dans les engrais d'oligo-éléments
Pour démontrer la conformité aux tolérances supérieures de l'ACIA pour les engrais représentés comme contenant des oligo-éléments, les demandeurs doivent soumettre les résultats d'analyse pour :
- Tout oligo-éléments garanti :
- bore (B)
- chlore (Cl)
- cuivre (Cu)
- fer (Fe)
- manganèse (Mn)
- molybdène (Mo)
- zinc (Zn)
Remarque : cette exigence relative à l'analyse des oligo-éléments s'ajoute à l'analyse des métaux décrite à la section 2.4.2.1.
Les résultats d'analyse doivent être soumis au moment de l'enregistrement et du réenregistrement afin de confirmer que la teneur réelle en oligo-éléments ne dépasse pas la quantité garantie au-delà de la tolérance admissible. Les limites de tolérance sont indiquées dans le tableau 10, à l'annexe 3.
Le nombre d'analyses requises est basé sur le nombre de lots produits au cours des cinq années précédant la demande, comme indiqué dans le tableau 4.
2.4.2.5 - Norme relative aux substances per- et polyfluoroalkyles (SPFA) pour les biosolides commerciaux
En vertu de la norme provisoire sur les SPFA, les engrais biosolides qui doivent être enregistrés doivent démontrer leur conformité à nos spécifications pour le sulfonate de perfluorooctane (SPFO).
Pour être importés ou vendus au Canada, ces produits doivent contenir moins de 50 parties par milliard (ppb) de SPFO sur la base du poids sec. Le SPFO est utilisé comme indicateur de contamination par les SPFA.
Documents requis
Les demandeurs doivent joindre les documents suivants à leur demande d'enregistrement :
- un rapport de laboratoire (certificat d'analyse) indiquant les résultats des tests de SPFO.
- un formulaire d'attestation dûment rempli
Pour le formulaire d'attestation, les directives d'échantillonnage et d'analyse, veuillez-vous reporter à la circulaire T-4-132 – Norme pour les substances per - et polyfluoroalkyles (SPFA) dans les biosolides commerciaux importés ou vendus au Canada comme engrai
2.4.3 - Justificatifs de l'innocuité et données complémentaires
Pour les produits nécessitant une évaluation complète de l'innocuité de niveau III, les demandeurs doivent fournir une justification scientifique de l'innocuité et toutes les données complémentaires nécessaires pour étayer l'innocuité du produit lorsqu'il est utilisé comme prévu. Ces évaluations suivent le cadre d'évaluation des risques en 4 étapes que nous utilisons ainsi que d'autres organismes de réglementation par exemple :
- Santé Canada
- Environnement Canada
- Agence de règlementation de la lutte antiparasitaire
- Environmental Protection Agency (EPA) des États-Unis
Les 4 étapes de l'évaluation des risques
- Identification du danger
Identification des effets néfastes potentiels sur la santé humaine ou l'environnement. - Évaluation de la relation dose-réponse
Évaluation de la relation entre la dose administré et la réponse biologique observée chez les individus ou les populations. - Évaluation de l'exposition
Estimation du niveau d'exposition des êtres humains, des animaux ou de l'environnement résultant de l'utilisation du produit, y compris l'absorption et les concentrations dans les milieux environnementaux. - Caractérisation des risques
Intégration des données relatives aux dangers et à l'exposition afin d'estimer la probabilité et la gravité des effets indésirables.
Risque = danger × exposition
Objectif de la justification de l'innocuité
La justification de l'innocuité doit démontrer que le produit, lorsqu'il est utilisé conformément aux instructions et sans dépasser son usage prévu, ne présente aucun risque inacceptable pour :
- la santé humaine
- la santé des plantes et des animaux
- l'environnement
Nous pouvons demander des renseignements supplémentaires en fonction du profil de risque du produit.
La justification relative à l'innocuité peut comporter jusqu'à 3 parties :
- profil de risque toxicologique
- profil de risque microbien
- références et documentation supplémentaire
Les demandeurs doivent fournir des informations scientifiques détaillées dans chaque section afin l'innocuité et la qualité de leur produit. Le niveau de détail requis doit être proportionnel au profil de risque du produit. Les produits à haut risque peuvent nécessiter des données et des justifications plus approfondies. Afin de s'assurer que la demande est complète et scientifiquement fondée, les demandeurs sont vivement encouragés à consulter des professionnels qualifiés en toxicologie et/ou en microbiologie avant de la soumettre.
Demandes de dérogation
S'il existe des raisons scientifiques de croire qu'une exigence d'information spécifique n'est ni nécessaire ni pertinente à l'évaluation de l'innocuité d'un produit ou d'un ingrédient, les demandeurs peuvent demander une dérogation.
Les demandes de dérogation doivent être accompagnées d'une justification scientifique solide.
2.4.3.1 - Profil de risque toxicologique
2.4.3.1.1 - Caractérisation des dangers toxicologiques
Pour les produits ou ingrédients dont l'innocuité n'est pas bien établie dans les engrais ou les suppléments, les demandeurs doivent remplir le tableau de caractérisation des dangers figurant à l'annexe 4.
Si certains éléments du tableau ne sont pas applicables ou pertinents, les demandeurs doivent fournir une justification scientifiquement fondée, avec des références bibliographiques, pour justifier leur exclusion.
Sources d'information
La caractérisation des dangers peut être fondée sur :
- la littérature scientifique évaluée par des pairs
- des bases de données réglementaires internationales
- études de toxicité in vitro ou in vivo
- modélisation prédictive (si les données expérimentales ne sont pas disponibles)
- des données de substitution (provenant de substances similaires), accompagnées d'une justification démontrant la similitude des propriétés physiques, chimiques et toxicologiques
Voir l'annexe 10 pour des sources d'informations utiles à l'appui de la détermination des dangers.
Considérations supplémentaires
Les demandeurs doivent identifier tout ce qui est connu :
- autres paramètres de danger (par exemple, l'allergénicité)
- dangers spécifiques à une voie d'exposition (par exemple, cancérogénicité pulmonaire due à une inhalation chronique)
- dangers spécifiques à certaines espèces (par exemple, la toxicité aviaire)
Nous pouvons demander des données supplémentaires en fonction des risques identifiés.
Ingrédients à risque élevé
Un ingrédient est considéré comme présentant un risque élevé s'il répond à 1 ou plusieurs des critères suivants (voir l'annexe 4 pour les définitions complètes) :
- toxicité aiguë élevée
- DL50 ≤ 500 mg/kg (par voie orale)
- CL50 ≤ 1 500 mg/m³ (inhalation)
- toxicité subchronique
- DSE(N)O ≤ 30 mg/kg p.c./jour
- DME(N)O ≤ 90 mg/kg p.c./jour
- toxicité chronique
- DSE(N)O ≤ 10 mg/kg p.c./jour
- DME(N)O ≤ 30 mg/kg p.c./jour
- résultats positifs pour:
- Cancérogénicité
- Clastogénicité
- Mutagénicité
- Toxicité pour la reproduction ou le développement
- Tératogénicité
- Perturbation endocrinienne
- toxicité aquatique aiguë élevée
- Plus faible CE50/CL50 moins de 0,1 ppm
Si l'un de ces critères est rempli, une évaluation toxicologique de l'exposition et une évaluation des risques doivent être réalisées (voir sections 2.4.3.1.2 et 2.4.3.1.3).
Ingrédients à faible risque
Les ingrédients qui ne répondent à aucun des critères de danger ne nécessitent pas d'évaluation de l'exposition ou des risques. Il n'est pas nécessaire de remplir les sections 2.4.3.1.2 et 2.4.3.1.3 pour ces ingrédients.
2.4.3.1.2 - Évaluation de l'exposition toxicologique
Les demandeurs doivent remplir l'annexe 5 pour tous les matériaux qui répondent aux critères de danger élevé décrits à l'annexe 4. Cela comprend :
- les ingrédients actifs et inertes
- les résidus
- les contaminants
- les produits de dégradation
Voies d'exposition à prendre en compte
Les voies d'exposition directes et indirectes doivent être prises en compte :
- Exposition directe :
- mélangeur professionnel
- chargeur
- applicateur/utilisateur
- Exposition indirecte:
- passant
- contamination des eaux souterraines
- résidus sur les cultures vivrières ou fourragères
- contact avec ou ingestion de sol contaminé
Facteurs influençant l'exposition
La pertinence de chaque voie d'exposition dépend :
- du mode d'utilisation prévu (par exemple, champ agricole ou terreau)
- les espèces cibles (par exemple, cultures ornementales ou cultures vivrières)
- la fréquence et le taux d'application
- les propriétés physicochimiques du produit et de ses composants
Ces facteurs doivent être clairement identifiés dans l'annexe 5 et utilisés pour définir des scénarios d'exposition réalistes.
Scénarios les plus défavorables et considérations relatives à l'étiquetage
Les demandeurs doivent tenir compte des pires scénarios d'exposition, notamment :
- utilisation par des applicateurs professionnels (considérée comme la fréquence d'exposition la plus élevée par l'ACIA)
- mentions sur l'étiquette qui limitent l'exposition, telles que :
- recommandations relatives à l'équipement de protection individuelle (EPI)
- instructions pour une manipulation et une élimination sécuritaire
- mentions de précaution
- restrictions d'utilisation (p. ex. « Ne pas utiliser sur les cultures vivrières ou les pâturages »)
- intervalles post-entrée, le cas échéant
Ces éléments figurant sur l'étiquette doivent être intégrés dans les estimations d'exposition afin de refléter des stratégies d'atténuation réalistes.
2.4.3.1.3 - Évaluation des risques toxicologiques
Les demandeurs doivent caractériser le risque toxicologique pour chaque ingrédient à risque élevé en intégrant la caractérisation des dangers et l'évaluation de l'exposition dans tous les scénarios d'exposition pertinents. La caractérisation des risques doit être documentée à l'annexe 5.
Nous examinerons et validerons les caractérisations des risques soumises. Si nécessaire, des données supplémentaires pourront être demandées afin de préciser les évaluations de danger ou d'exposition. Nous pourrons également exiger des mesures d'atténuation des risques afin de garantir une utilisation sécuritaire du produit, notamment :
- l'utilisation d'équipements de protection individuelle (EPI)
- des procédures de manipulation et d'élimination sécuritaires
- des mentions de précaution sur l'étiquette
- des restrictions d'utilisation (par exemple, cultures vivrières et cultures non vivrières )
- intervalles postérieurs à l'entrée, le cas échéant
2.4.3.2 - Profil de risque microbiologique
2.4.3.2.1 - Évaluation du danger microbiologique
Pour les produits ou ingrédients dont l'innocuité dans les engrais ou les suppléments n'est pas bien établie, les demandeurs doivent procéder à une évaluation des risques microbiologiques. L'objectif est de caractériser chaque micro-organisme et d'identifier les effets néfastes potentiels de sur les humains, les animaux, les plantes et l'environnement. Ces effets peuvent inclure, sans s'y limiter :
- la pathogénicité
- la toxicité
- la sensibilisation
- la toxigénicité
- la résistance aux antimicrobiens
Les dangers peuvent provenir du micro-organisme lui-même, de ses métabolites ou toxines, ou de son matériel génétique.
Pour appuyer l'évaluation des risques, les demandeurs doivent recueillir des informations auprès de sources fiables, telles que :
- données d'essais expérimentaux
- études de cas
- littérature scientifique évaluée par des pairs
- projets de recherche achevées ou en cours
Si les données sur un micro-organisme sont limitées, les demandeurs peuvent utiliser un organisme de substitution scientifiquement justifié, à condition que la justification soit clairement documentée.
L'évaluation doit tenir compte des facteurs spécifiques à la souche et de tous les stades de vie du micro-organisme, car ceux-ci peuvent influencer la gravité du danger.
Dans la mesure du possible, les demandeurs doivent fonder leur évaluation des effets indésirables sur des données d'essais ou d'études spécifiques au micro-organisme. Conformément au Cadre d'évaluation des risques microbiens (CERM) en vertu du Règlement sur les renseignements concernant les substances nouvelles (organismes) de la Loi canadienne sur la protection de l'environnement (1999), les essais doivent commencer à la dose maximale indiquée sur l'étiquette. Si des effets indésirables sont observés, les demandeurs doivent effectuer des essais supplémentaires à des doses plus faibles afin d'établir une relation dose-réponse et de déterminer les principaux critères d'évaluation statistiques, tels que :
- DI50/CI50– Dose Infectieuse médiane / Concentration Infectieuse médiane
- DE50/CE50– Dose Efficace médiane / Concentration Efficace médiane
- DL50/CL50– Dose Létale médiane / Concentration Létale médiane
Les demandeurs sont invités à consulter le guide d'Environnement Canada intitulé Guide des essais de pathogénicité et de toxicité de nouvelles substances microbiennes pour les organismes aquatiques et terrestres (deuxième édition, 2016) pour connaître les méthodologies recommandées.
Les demandeurs doivent se reporter à l'annexe 6 pour obtenir une liste détaillée des données requises pour la caractérisation des dangers microbiens. Il est recommandé d'utiliser l'annexe 6 comme liste de contrôle afin de s'assurer que le dossier est complet. Toutes les informations présentées doivent être correctement référencées et des copies des publications, documents ou rapports d'étude cités doivent être incluses dans la soumission.
L'annexe 11 fournit les références citées dans cette section et des ressources supplémentaires à l'appui de l'évaluation des dangers.
2.4.3.2.2 - Évaluation de l'exposition microbiologique
Les demandeurs doivent réaliser une évaluation de l'exposition afin de déterminer comment le micro-organisme peut pénétrer dans l'environnement récepteur et de caractériser son devenir et son comportement dans l'environnement. L'évaluation doit déterminer l'exposition potentielle pour l'homme et l'environnement en termes de :
- la probabilité
- l'ampleur
- la fréquence
- la durée
- l'étendue
L'exposition directe (p. ex. le contact avec le produit) et l'exposition indirecte (p. ex. le rejet dans l'environnement lors des utilisations prévues) doivent être évaluées.
Pour l'exposition indirecte, les demandeurs doivent évaluer :
- le devenir du micro-organisme
- son matériel génétique, ses toxines et ses métabolites
- son potentiel endophyte
- la probabilité d'apparition dans la partie comestible de la culture
Si les données sur le micro-organisme spécifique sont limitées, les demandeurs peuvent utiliser un substitut scientifiquement justifié, en documentant clairement leur raisonnement et en l'appuyant par des références.
Les demandeurs doivent se reporter à l'annexe 7, qui présente les principaux éléments à prendre en considération pour caractériser l'exposition microbiologique. Il est recommandé d'utiliser l'annexe 7 comme liste de contrôle afin de s'assurer que tous les facteurs pertinents liés à l'exposition sont pris en compte.
2.4.3.2.3 - Évaluation des risques microbiologiques
Les demandeurs doivent fonder la conclusion de l'évaluation des risques à la fois sur le danger caractérisé et sur les informations disponibles concernant l'exposition.
Pour faciliter ce processus, l'annexe 8 résume les considérations clés pour classer la gravité des dangers microbiologiques et le niveau d'exposition.
Lorsque la caractérisation des risques indique un risque potentiel pour la santé humaine ou l'environnement, des mesures d'atténuation des risques peuvent être nécessaires. Ces mesures peuvent inclure, sans s'y limiter :
- l'utilisation d'équipements de protection individuelle (EPI)
- la mise en œuvre de procédures de manipulation et d'élimination sûres
- l'ajout de mentions de précaution sur les étiquettes
- des restrictions d'utilisation, telles que :
- l'interdiction d'application sur les cultures vivrières
- les pâturages
- les zones de pâturage
- l'établissement d'intervalles post-entrées afin de réduire l'exposition des travailleurs et des personnes présentes
Les demandeurs doivent identifier et proposer des mesures d'atténuation appropriées en fonction de la nature et de la gravité du risque. Nous examinerons les mesures proposées et pourra demander des contrôles supplémentaires afin de garantir l'utilisation sécuritaire du produit.
2.4.3.3 - Références et documentation supplémentaire
Toutes les informations publiées utilisées pour satisfaire aux exigences en matière d'évaluation des risques pour l'innocuité, justification de l'innocuité (onglet 5) doivent être :
- citées dans le texte en indiquant l'auteur/la source et l'année
- répertoriées dans une section de références sous cet onglet, avec les détails complets de la citation
- auteurs
- nom du document
- source
- date
- numéros de page
Les demandeurs doivent également fournir :
- des copies de tous les documents référencés qui ne sont pas accessibles au public (c'est-à -dire qui ne sont pas accessibles via des liens en libre accès)
- des liens directs vers les sources en libre accès, lorsqu'elles sont disponibles – le téléchargement n'est pas nécessaire pour les documents accessibles au public
- les résultats analytiques utilisés ou mentionnés dans les onglets 4 et 5
- références de tous les modèles ou logiciels de modélisation utilisés pour appuyer le raisonnement en matière d'innocuité (y compris le nom et la version du modèle), à la fois dans le texte et dans la liste de références sous cet onglet
2.5. Nom et adresse du fabricant
Les demandeurs doivent fournir le nom légal de la personne ou de la société responsable de la fabrication du produit final ou du supplément. En outre, les demandeurs doivent indiquer l'adresse complète du site de fabrication et non celle du siège social ou de la société.
Si le produit ou le supplément est fabriqué sur plusieurs sites, les demandeurs doivent indiquer le nom légal de chaque fabricant et l'adresse correspondante du site de fabrication.
Ces informations sont essentielles pour vérifier l'origine du produit et garantir la conformité aux exigences réglementaires.
Des informations incomplètes ou inexactes peuvent retarder le processus d'examen.
2.6. Étiquette proposée pour le marché
Toute personne qui emballe ou fait emballer un engrais ou un supplément, ou qui importe un engrais ou un supplément emballé, doit s'assurer que l'emballage est étiqueté conformément au Règlement sur les engrais.
Une copie de l'étiquette proposée pour le produit, ou l'intégralité du texte qui devrait figurer sur l'étiquette du produit, doit être jointe à la demande d'enregistrement. Nous accepterons les versions en texte seul pendant les étapes initiales de l'examen, mais n'enregistrera pas le produit sans avoir examiné et approuvé l'étiquette finale destinée au marché.
Toutes les informations requises par le règlement doivent être imprimées de manière visible, lisible et indélébile, en anglais et en français.
L'étiquette du produit doit :
- ne contenir aucune information ou aucun symbole incorrect ou trompeur qui pourrait raisonnablement induire l'acheteur en erreur concernant :
- l'identité du produit en tant qu'engrais ou supplément
- sa sécurité
- sa composition
- son mode d'emploi
- être cohérente avec toutes les informations fournies lors du processus d'enregistrement
- définir clairement tous les acronymes utilisés
- utilisez les unités de mesure métriques
Les unités impériales équivalentes peuvent apparaître en plus des unités métriques (la conversion doit être exacte).
Pour obtenir des renseignements complets sur les exigences en matière d'étiquetage, y compris des exemples d'étiquettes, veuillez consulter la circulaire T-4-130 – Exigences en matière d'étiquetage des engrais et des suppléments.
Mises en garde supplémentaires pour les étiquettes
Les étiquettes des engrais ou des suppléments réglementés doivent comporter des mentions visant à atténuer les risques pour la santé humaine, animale ou végétale, ou pour l'environnement. La circulaire T-4-130 décrit les mises en garde requises lorsque certains ingrédients sont présents ou peuvent être présents.
Afin d'aider les demandeurs à concevoir des étiquettes pour l'enregistrement, les exemples suivants illustrent les mises en garde supplémentaires qui peuvent être requises au-delà de la circulaire T-4-130, en fonction des concentrations des ingrédients et/ou des modes d'utilisation. Ces mises en garde sont évaluées au cas par cas et sont fournies ici à titre indicatif uniquement.
Exemples :
- produits contenant des concentrations élevées de sucre (par exemple, de la mélasse) et destinés à une application foliaire ou par fertigation, où l'application peut augmenter le risque de bactéries pathogènes liées à des maladies d'origine alimentaire
- Mention obligatoire :
- Ne pas utiliser sur les légumes-feuilles, les fruits ou les légumes dans les 10 jours précédant la récolte et
- Ne pas appliquer à l'aide d'un système d'irrigation.
- Mention obligatoire :
- produits contenant de l'uréase ou des inhibiteurs de nitrification, lorsque les instructions d'application n'excluent pas explicitement les pâturages ou les terres de pâturage. Ces produits peuvent présenter un risque pour le bétail s'ils sont ingérés directement ou par contact avec les zones traitées
- Mention obligatoire :
- Ne pas utiliser dans l'alimentation du bétail. Tenir le bétail à l'écart des zones traitées pendant 14 jours ou jusqu'à ce que 25 mm (1 pouce) de pluie se soient accumulés. L'urée et l'UAN peuvent être toxiques pour le bétail en cas d'ingestion.
- Mention obligatoire :
- produits de traitement des semences contenant du graphite et/ou du talc
- Afin de soutenir l'interdiction par l'ARLA de l'utilisation de graphite et de talc avec les insecticides néonicotinoïdes et ainsi permettre une utilisation sécuritaire des produits, la déclaration suivante est requise
- Contient [graphite et/ou talc]. Lors de l'utilisation de ce produit en combinaison avec des insecticides, suivez attentivement toutes les directives pour une utilisation sécuritaire.
- Afin de soutenir l'interdiction par l'ARLA de l'utilisation de graphite et de talc avec les insecticides néonicotinoïdes et ainsi permettre une utilisation sécuritaire des produits, la déclaration suivante est requise
3.0. Coordonnées
Section de l'innocuité des engrais
c/o Bureau de présentation des demandes préalables à la mise en marché (BPDPM)
Agence canadienne d'inspection des aliments
1400 chemin Merivale
Ottawa (Ontario) K1A 0Y9
Canada
Téléphone : 1-855-212-7695
Télécopieur : 613-773-7115
Courriel :cfia.paso-bpdpm.acia@inspection.gc.ca
Annexes
Annexe 1 : Format de demande d'enregistrement d'un produit
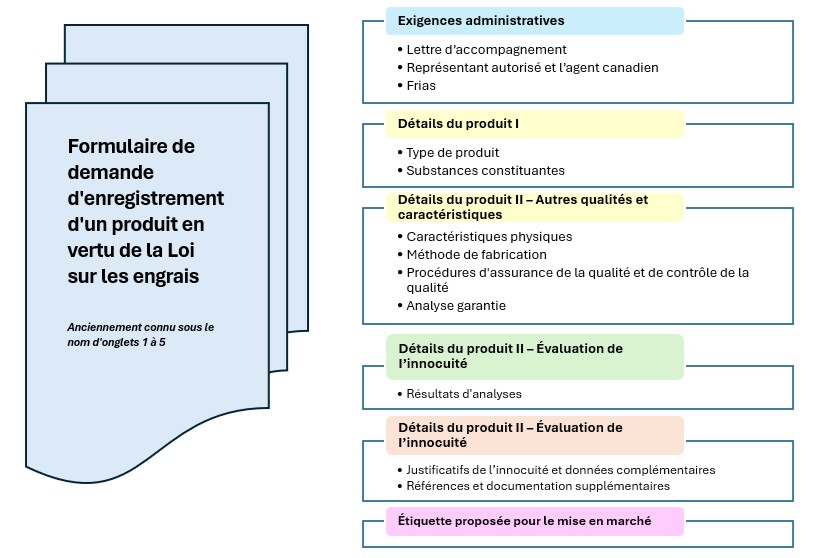
Description du graphique - Format de demande d'enregistrement d'un produit
- Exigences administratives
- Lettre d'accompagnement
- Représentant(s) autorisé(s) et agent canadien
- Frais
- Détails du produit I
- Type de produit
- Substances constituents
- Détails du produit II – autres qualités et caractéristiques
- Caractéristiques physiques
- Méthode de fabrication
- Procédures d'assurance de la qualité et de contrôle de la qualité
- Analyse garantie
- Détails du produit II – évaluation de l'innocuité
- Résultats de l'analyse
- Détails du produit II – Évaluation de l'innocuité
- Justification de l'innocuité et données complémentaires
- Références et documentation supplémentaire
- Étiquette commerciale
Annexe 2 : Exigences propres aux ingrédients pour démontrer leur innocuité
Les exigences en matière de données d'innocuité varient en fonction de la nature et du profil de risque du produit. La présence d'ingrédients actifs ou inertes peut nécessiter des documents d'innocuité supplémentaires. Le tableau ci-dessous présente les ingrédients courants des produits et les exigences en matière de données d'innocuité qui leur sont associées. Tous les produits contenant des sous-produits industriels ou des matières organiques recyclées doivent être accompagnés de résultats d'analyses.
Tableau 5. Résumé des exigences en matière d'information pour divers ingrédients de produits
Remarque : cette liste n'est pas exhaustive et ne couvre pas toutes les exigences spécifiques aux produits/ingrédients.
| - | Produit Détails I-II | Analyses requises | Évaluation des risques pour la sécurité | ||
|---|---|---|---|---|---|
| Métaux | Dioxines et composés de type dioxine | Organismes indicateurs | |||
| Acide indole-3-butyrique (AIB) présent à une concentration ne dépassant pas 1 % dans le produit, à l'exception des produits destinés à être pulvérisés | cocher | - | - | - | - |
| MVA (mycorhizes à vésicules etarbuscules), si l'espèce est essentiellement équivalente ou représentative du groupe des MVA | cocher | - | - | - | - |
| Rhizobia (espèces des genres Rhizobium, Bradyrhizobium, Mesorhizobium et Sinorhizobium) à condition que l'espèce soit représentative du groupe des rhizobiums et qu'elle ne soit pas génétiquement modifiée. | cocher | - | - | - | - |
| Bacillus subtilis, à condition que la souche soit représentative de l'espèce, qu'elle ne soit pas génétiquement modifiée et qu'elle ne produise aucune entérotoxine humaine. | cocher | - | - | - | - |
| - | Produit Détails I-II | Analyses requises | Évaluation des risques pour la sécurité | ||
|---|---|---|---|---|---|
| Métaux | Dioxines et composés de type dioxine | Organismes indicateurs | |||
| Nutriments d'origine minérale | cocher | cocher | - Note de tableau a | - | - |
| Oligo-éléments | cocher | cocher | - Note de tableau a | - | - |
| Extraits et résidus végétaux | cocher | cocher | - | cocher | - |
| Algues | cocher | cocher | - | cocher | - |
| Acides aminés | cocher | cocher | - | cocher | - |
| Engrais contenant | - | - | - | - | - |
|
Sous-produits du ciment |
cocher | cocher Note de tableau b | cocher | - | - |
|
Compost |
cocher | cocher | - | cocher | - |
|
Farines |
cocher | cocher | - | cocher | - |
| Matières d'égouts traitées compostées ou pas | cocher | cocher | cocher | cocher | - |
|
Boues de pâte à papier et de papier |
cocher | cocher | cocher | cocher | - |
|
Cendres de bois |
cocher | cocher | cocher | - | - |
|
Déchets organiques |
cocher | cocher | - | cocher | - |
| Silice | cocher | cocher | - | - | - |
| Engrais à base de poisson ou de crustacés | cocher | cocher | - | cocher | - |
| Turricule | cocher | cocher | - | cocher | - |
| - | Produit Détails I-II | Analyses requises | Évaluation des risques pour la sécurité | ||
|---|---|---|---|---|---|
| Métaux | Dioxines et composés de type dioxine | Organismes indicateurs | |||
| Engrais enrobés de polymers | cocher | - | - | - | cocher |
| Polymères stabilisateurs de sol | cocher | - | - | - | cocher |
| Agents mouillants et surfactants | cocher | - | - | - | cocher |
| Produits composés de nanomatériaux (en tout ou en partie) | cocher | - | - | - | cocher |
| Vitamines | cocher | - | - | - | cocher |
| Inhibiteurs de nitrification et d'uréase | cocher | - | - | - | cocher |
| Régulateurs de croissance des plantes et composés de signalisation végétale (par exemple la gibbérelline, les cytokines, le NAA, les LCO, l'acide salicylique, le chitosane, l'hespérétine, la naringénine) autres que l'AIB de niveau I décrit ci-dessus | cocher | - | - | - | cocher |
| Suppléments enregistrables qui requièrent un ensemble complet de données d'innocuité, mélangés à l'engrais. | cocher | Note de tableau a | Note de tableau a | Note de tableau a | cocher |
| Micro-organismes viables autres que ceux décrits dans le niveau I | cocher | - | - | cocher | cocher |
| Métabolites d'organismes | cocher | - | - | cocher | cocher |
Annexe 3 : Normes et seuils relatifs aux métaux, aux dioxines et aux composés de type dioxine et niveaux maximaux acceptables d'organismes indicateurs dans les engrais et les suppléments
Normes relatives aux métaux
Les métaux préoccupants comprennent :
- l'arsenic (As)
- le cadmium (Cd)
- le chrome (Cr)
- le cobalt (Co)
- le cuivre (Cu)
- le mercure (Hg)
- le molybdène (Mo)
- le nickel (Ni)
- le plomb (Pb)
- e sélénium (Se)
- le zinc (Zn)
Une accumulation de ces métaux dans le sol à long terme peut mener à une toxicité végétale, animale, environnementale ou humaine. La concentration maximale permise de métaux dans un produit dépend du taux d'application de ce dernier.
Les normes pour les métaux sont fixées en fonction du maximum admissible d'ajouts cumulatifs au sol sur une période de 45 ans et non par rapport aux concentrations réelles de métaux dans les produits. Le taux d'application d'un produit est un élément essentiel pour déterminer les concentrations de métaux acceptables dans ce dernier. L'approche de l'application cumulative de 45 ans vise à tenir compte de la persistance des métaux dans l'environnement, ce qui, ultimement, détermine le niveau de contamination et donc, les répercussions à long terme.
Calcul de la concentration maximale acceptable de métaux
La concentration maximale acceptable de chaque métal (en mg de métal/kg de produit) est calculée à l'aide de nos normes relatives aux ajouts maximaux acceptables dans le sol et au taux d'application annuel maximal recommandé pour le produit.
Tous les engrais et suppléments, y compris les eaux usées traitées, les composts et autres sous-produits, doivent respecter les normes relatives aux ajouts cumulatifs maximaux acceptables de métaux dans le sol.
La formule est la suivante :
Considérations relatives aux métaux nutritifs
Certains métaux tels que :
- le cuivre (Cu),
- le molybdène (Mo)
- le zinc (Zn) sont des éléments nutritifs essentiels pour les plantes.
Les produits qui garantissent ces éléments nutritifs pour corriger les carences ne sont pas tenus d'indiquer un taux d'application sur l'étiquette, mais celle-ci doit préciser que le taux d'application doit être basé sur une analyse du sol ou des tissus. Dans ces cas, les concentrations de métaux peuvent dépasser la norme en métaux (en raison de la fréquence limitée d'application) et le 95e centile des taux d'application agronomiques recommandés au niveau provincial pour les nutriments garantis est utilisé dans les calculs.
Le tableau 6 indique les concentrations acceptables de métaux pour les produits à différents taux d'application.
| Métal | Maximum admissible d'ajouts cumulatifs de métaux au sol sur une période de 45 ans (kg de métal/ha) |
Exemples de concentrations maximales admissibles de métaux dans les produits en fonction des taux d'application annuels (mg de métal/kg de produit) |
||
|---|---|---|---|---|
| 4 400 kg/ha par an | 2 000 kg/ha par an | 500 kg/ha par an | ||
| Arsenic (As) | 15 | 75 | 166 | 666 |
| Cadmium (Cd) | 4 | 20 | 44 | 177 |
| Chrome (Cr) | 210 | 1 060 | 2 333 | 9 333 |
| Cobalt (Co) | 30 | 151 | 333 | 1 333 |
| Cuivre (Cu) | 150 | 757 | 1 666 | 6 666 |
| Mercure (Hg) | 1 | 5 | 11 | 44 |
| Molybdène (Mo) | 4 | 20 | 44 | 177 |
| Nickel (Ni) | 36 | 181 | 400 | 1 600 |
| Plomb (Pb) | 100 | 505 | 1 111 | 4 444 |
| Sélénium (Se) | 2.8 | 14 | 31 | 124 |
| Thallium (Tl) Note de tableau a | 1 | 5 | 11 | 44 |
| Vanadium (V) Note de tableau a | 130 | 656 | 1 444 | 5 777 |
| Zinc (Zn) | 370 | 1 868 | 4 111 | 16 444 |
Remarques supplémentaires
- Le taux d'application et la concentration en métaux doivent être exprimés sur la même base (par exemple, tous deux sur la base du poids sec ou tous deux « tels quels »).
- Le Conseil canadien des ministres de l'environnement (CCME), le Bureau de normalisation du Québec (BNQ) et diverses provinces ont également établi des lignes directrices concernant
- les métaux dans les sols
- les boues
- le compost
- d'autres produits
Pour plus d'informations, veuillez contacter votre gouvernement provincial.
- Le sélénium et le cobalt sont considérés comme des ingrédients actifs de supplément, car ils ne sont pas des nutriments essentiels pour toutes les espèces végétales. Leur inclusion dans la formulation d'un engrais fait de ce produit un engrais enregistrable contenant un supplément.
- Outil de conformité : Un outil de vérification de la conformité (tableau Excel) est disponible sur demande à l'adresse paso-bpdpm.acia@inspection.gc.ca. Cet outil automatise les calculs des normes relatives aux métaux et aide les fabricants, les requérants et les inspecteurs de l'ACIA à vérifier la conformité des produits.
Normes relatives aux dioxines et aux composés de type dioxine
Exemples de contaminants environnementaux très persistants :
- les dibenzo-p-dioxines polychlorées (PCDD)
- les dibenzofuranes polychlorés (PCDF)
- les polychlorobiphényles (PCB) de type dioxine
En raison de leur nature lipophile, ils sont connus pour se bioaccumuler dans les chaînes alimentaires. Ces composés sont associés à toute une série d'effets toxiques chez les humains et les animaux, notamment :
- la cancérogénicité
- l'immunotoxicité
- la toxicité pour la reproduction et le développement
- la perturbation endocrinienne.
Leur persistance et leur capacité à se concentrer dans les tissus adipeux les rendent particulièrement préoccupants pour leurs effets à long terme sur l'environnement et la santé.
La norme de l'ACIA pour l'ajout cumulatif maximal acceptable de dioxines et de composés de type dioxine dans le sol est la suivante :
5,355 mg ET/ha sur 45 ans
(E = équivalent toxique).
Comme pour les métaux, le taux d'application du produit est un facteur clé pour déterminer les concentrations acceptables. L'approche d'application cumulative sur 45 ans tient compte de la persistance environnementale et des effets à long terme de ces composés. Le tableau 7 répertorie les congénères à analyser pour déterminer la concentration totale de dioxines et de composés de type dioxine dans un produit.
Les congénères suivants doivent être analysés pour déterminer la concentration totale en dioxines et composés de type dioxine dans un produit :
| Composé | Facteur d'équivalence toxique (FET) |
|---|---|
| Dibenzo-p-dioxines chlorées (PCDD) | |
| 2,3,7,8-TCDD | 1 |
| 1,2,3,7,8-PCDD | 1 |
| 1,2,3,4,7,8-HCDD | 0,1 |
| 1,2,3,6,7,8-HCDD | 0,1 |
| 1,2,3,7,8,9-HCDD | 0,1 |
| 1,2,3,4,6,7,8-HCDD | 0,01 |
| OCDD | 0,0001 |
| Composé | Facteur d'équivalence toxique (FET) |
|---|---|
| Dibenzofuranes chlorés (PCDF) | |
| 2,3,7,8-TCDF | 0,1 |
| 1,2,3,7,8-PCDF | 0,05 |
| 2,3,4,7,8-PCDF | 0,5 |
| 1,2,3,4,7,8-HCDF | 0,1 |
| 1,2,3,6,7,8-HCDF | 0,1 |
| 1,2,3,7,8,9-HCDF | 0,1 |
| 2,3,4,6,7,8-HCDF | 0,1 |
| 1,2,3,4,6,7,8-HCDF | 0,01 |
| 1,2,3,4,7,8,9-HCDF | 0,01 |
| OCDF | 0,0001 |
| Composé | Facteur d'équivalence toxique (FET) | |
|---|---|---|
| PCB non-ortho substitués | ||
| 3,3',4,4'-PCB | PCB n° 077 | 0,0001 |
| 3,4,4',5-PCB | PCB n° 081 | 0,0003 |
| 3,3',4,4',5-PCB | PCB n° 126 | 0,1 |
| 3,3',4,4',5,5'-PCB | PCB n° 169 | 0,03 |
| Composé | Facteur d'équivalence toxique (FET) | |
|---|---|---|
| PCB mono-ortho substitués | ||
| 2,3,3',4,4'-PCB | PCB n° 105 | 0,00003 |
| 2,3,4,4',5-PCB | PCB n° 114 | 0,00003 |
| 2,3',4,4',5-PCB | PCB n° 118 | 0,00003 |
| 2',3,4,4',5-PCB | PCB n° 123 | 0,00003 |
| 2,3,3',4,4',5-PCB | PCB n° 156 | 0,00003 |
| 2,3,3',4,4',5'-PCB | PCB n° 157 | 0,00003 |
| 2,3',4,4',5,5'-PCB | PCB n° 167 | 0,00003 |
| 2,3,3',4,4',5,5'-PCB | PCB n° 189 | 0,00003 |
| Composé | Facteur d'équivalence toxique (FET) | |
|---|---|---|
| Indicateur-PCB | ||
| 2,4,4'-PCB | PCB n° 028 | 0,000002 |
| 2,2',5,5'-PCB | PCB n° 052 | 0,000005 |
| 2,2',4,5,5'-PCB | PCB n° 101 | 0,00003 |
| 2,2',3,4,4',5'-PCB | PCB n° 138 | 0,00002 |
| 2,2',4,4',5,5'-PCB | PCB n° 153 | 0,00001 |
| 2,2',3,4,4',5,5'-PCB | PCB n° 180 | 0,000005 |
Calcul de la concentration acceptable dans les produits
La concentration maximale acceptable de dioxines et de composés de type dioxine dans les produits (en ng ET/kg de produit) est calculée à l'aide de la norme cumulative d'ajout au sol de l'ACIA : 5,355 mg ET/ha sur 45 ans et du taux d'application annuel maximal recommandé pour le produit, comme suit :
De plus, on considère une concentration maximale dans le produit de 100 ng ET/kg de produit afin de protéger les travailleurs et les autres personnes exposées.
Le tableau 8 indique les concentrations acceptables de dioxines/furanes pour les produits à différents taux d'application.
| Taux d'application | Concentration maximale acceptable (ng ET/kg de produit) |
|---|---|
| 4 400 kg/ha/an | 27 |
| 2 000 kg/ha/an | 59,5 |
Outil de conformité
Un outil de vérification de la conformité est disponible sur demande à l'adresse suivante : cfia.paso-bpdpm.acia@inspection.gc.ca
Ce calculateur Excel comprend une fonctionnalité permettant d'évaluer les limites pour les polluants organiques persistants, y compris les dioxines et les composés de type dioxine.
Organismes indicateurs
La surveillance des organismes indicateurs dans les engrais et les suppléments est nécessaire pour démontrer l'efficacité des processus de réduction des agents pathogènes et pour évaluer la qualité microbienne du produit final.
Conformément à la partie 503 de l'Environmental Protection Agency (EPA) des États-Unis, nous utilisons Salmonella spp. et les coliformes fécaux comme organismes indicateurs. Ceux-ci ont été sélectionnés en raison de leur présence répandue dans l'environnement et de leur fiabilité dans l'identification de la contamination microbienne.
Salmonella est reconnue comme un agent pathogène préoccupant, tandis que les coliformes fécaux sont faciles à cultiver et à quantifier, ce qui en fait des indicateurs efficaces et acceptables de la contamination fécale. La recherche de ces organismes permet également de détecter la repousse bactérienne après le traitement, ce qui facilite la validation des contrôles d'innocuité microbienne appliqués pendant la production.
| Organisme indicateur | Niveau maximal | Limite de detection minimale |
|---|---|---|
| Salmonella | Non détectable | moins de 1 UFC (unité formant colonie) / 25 grammes |
| Coliformes fécaux | 1000 MPN (nombre le plus probable) / gramme solide | moins de 2 UFC / gramme |
Remarque : les analyses pour les organismes indicateurs doivent respecter les limites minimales de détection spécifiées dans le tableau 9.
Conseils supplémentaires
Un outil de vérification de la conformité est disponible sur demande auprès de l'cfia.paso-bpdpm.acia@inspection.gc.ca. Le calculateur comprend une fonctionnalité pour les limites des organismes indicateurs.
Nous nous réservons le droit d'exiger des analyses visant à détecter d'autres organismes pathogènes, selon la nature du produit, évaluée au cas par cas.
Les demandeurs sont invités à consulter le Compendium des analyses microbiologiques de Santé Canada pour obtenir des exemples de méthodes standard reconnues. Pour être considérée comme acceptable, une méthode doit démontrer les éléments suivants pour la détection du principe actif dans le produit formulé :
- spécifique
- sélective
- fiable
- précise
Tolérances supérieures pour les garanties en oligo-éléments
Afin de favoriser une utilisation sûre et de faciliter la vérification de la conformité tant lors de l'évaluation préalable à la mise en marché que lors de la surveillance et de l'application de la réglementation sur le marché, des tolérances maximales ont été établies pour les garanties d'oligo-éléments. Ces tolérances tiennent compte de la variabilité analytique dans l'analyse des produits et des erreurs d'échantillonnage, ainsi que de la faisabilité en fonction des procédés de fabrication modernes.
Pour une garantie donnée (colonne de gauche), le dépassement admissible est ajouté à la garantie afin de déterminer la teneur maximale admissible (colonne de droite).
| Intervalle de garantie (%) | Excédence de garantie permise |
|---|---|
| <0,0033 | 0,0013 |
| 0,0033-0,0099 | 0,0040 |
| 0,010-0,032 | 0,010 |
| 0,033-0,099 | 0,031 |
| 0,10-0,32 | 0,077 |
| 0,33-0,99 | 0,23 |
| 1,0-3,2 | 0,60 |
| 3,3-9,99 | 1,0 |
| ≥ 10 | 10 % de la garantie |
Veuillez noter que les tolérances varient dépendamment de l'intervalle de garanties des oligo-éléments – la tolérance est plus élevée dans les petits intervalles et la tolérance est plus petite lorsque la concentration dans le produit est plus élevée.
Exemples
Un produit avec une garantie de 0,24 % de Cu a un excédent permis de 0,077, ce qui donne une teneur maximale acceptable en Cu de 0,317 %.
Un produit avec une garantie de 11 % de Cu a un excédent permis de 10 % de la garantie, soit 1,1 %, ce qui donne une teneur maximale acceptable en Cu de 12,1 %.
Annexe 4 : Caractérisation des dangers toxicologiques
| - | Caractérisation |
|---|---|
| Ingrédient | - |
| Numéro CAS (Chemical Abstract Number) | - |
| Concentration relative dans le produit final | - |
| Critères de l'évaluation de l'exposition | Critères de risque Note de tableau a | Valeur | Référence(s) |
|---|---|---|---|
| Coefficient de répartition du carbone organique (Koc) | - | - | - |
| Logarithme du coefficient de partage n-octanol/eau (Log Kow) | - | - | - |
| Hydrosolubilité à 25 °C | - | - | - |
| Pression de vapeur | - | - | - |
| Persistance Air | ≥ 2 jours | - | - |
| Persistance Eau | ≥ 6 mois | - | - |
| Persistance Sol | ≥ 6 mois | - | - |
| Persistance Sédiments | ≥ 1 an | - | - |
|
Facteurs de bioconcentration |
> 5000 | - | - |
| Effet toxicologique en fonction de la voie d'exposition | Critères de classification du danger Note de tableau a | Organisme | Durée | Effet | Dose | Références | |
|---|---|---|---|---|---|---|---|
| Orale | Aiguë (DL50, DSEO, DSENO) | DL50 ≤ 500 mg/kg pc | - | - | - | - | - |
| Subchronique DME(N)O, DSE(N)O | DME(N)O ≤ 90 mg/kg pc | - | - | - | - | - | |
| DSE(N)O ≤ 30 mg/kg pc | - | - | - | - | - | ||
| Chronique DME(N)O, DSE(N)O | DME(N)O ≤ 30 mg/kg pc | - | - | - | - | - | |
| DSE(N)O ≤ 10 mg/kg pc | - | - | - | - | - | ||
| Cutanée | Aiguë (DL50, DSEO, DSENO) | DL50 ≤ 500 mg/kg pc | - | - | - | - | - |
| Irritation et sensibilisation | - | - | - | - | - | - | |
| Inhalation | Aiguë (DL50, DSEO, DSENO) | DL50 ≤ 1 500 mg/m3 | - | - | - | - | - |
| Occulaire | Irritation | - | - | - | - | - | - |
| Cancérogénicité | Pour chaque ingrédient répondant aux critères de danger procéder à l'appendice 5. | - | - | - | Note de tableau b | - | |
| Clastogénicité et mutagénicité | - | - | - | - | - | ||
| Toxicité reproductive et développementale, tératogénicitée | - | - | - | - | - | ||
| Perturbation endocrinienne | - | - | - | - | - | ||
| Catégorie | Critères de classification du danger Note de tableau a | Organisme | Durée | Effet | Concn | Références |
|---|---|---|---|---|---|---|
| Vertébrés (p. ex., la truite arc-en-ciel (Oncorhynchus mykiss), l'omble de fontaine (Salvelinaus fontinalis), la tête-de-boule (Pimephales promelas), le crapet arlequin (Lepomis macrochirus) | Aiguë : CE50 la plus faible ou CL50 < 0,1 ppm | - | - | - | - | - |
| Invertébrés (p. ex., la daphnie (Daphnia sp. Ceriodaphnia dubia), le poisson zèbre (Brachydanio rerio), le ver (Lumbriculus variegatus)) | Aiguë : CE50 la plus faible ou CL50 < 0,1 ppm | - | - | - | - | - |
| Benthiques (p. ex., l'amphipode (Hyallela azteca), les larves de moucheron (Chironomus tentans, Chironomus riparius)) | Aiguë : CE50 la plus faible ou CL50 < 0,1 ppm | - | - | - | - | - |
| Algues (p. ex., Pseudokrchneriella subcapitata, Champia parvula) | Aiguë : CE50 la plus faible ou CL50 < 0,1 ppm | - | - | - | - | - |
Annexe 5 : Évaluation de l'exposition et du risque toxicologique
À remplir uniquement pour les ingrédients à haut risque (ceux qui répondent à l'un des critères de danger identifiés à l'annexe 4)
Mélangeur/applicateur
| - | Hypothèse/calcul/justification |
|---|---|
| Méthodologie et équipement d'application | - |
| Taux d'application | - |
| Aire d'application (ha) | - |
| Fréquence d'application | - |
| Voies d'exposition prévues (par exemple, voie cutanée et inhalation) basée sur la méthode d'application, le produit et les propriétés physico-chimiques constituantes |
- |
| Facteurs d'atténuation qui limitent l'exposition | - |
|
Équipement de protection individuel (EPI) |
- |
|
Facteur d'absorption cutané (le cas échéant) (% de la dose orale) (FAC) |
Fournir une valeur et la référence connexe |
| Estimation de l'exposition, α (mg/kg pc/j) | Présenter le calcul et les hypothèses de modélisation associées |
| - | Hypothèse/calcul/justification |
|---|---|
| Effet critique et dose critique, β (mg/kg pc/j) et/ou Coefficient de pouvoir cancérogène, ql* (mg/kg pc/j)-1 |
Tels qu'indiqués à l'annexe 4 |
| Marge d'innocuité (α/β) et/ou Risque additionnel de cancer (RAC) (q1* x α) |
- |
Autres personnes exposées/exposition indirect
| - | Hypothèse/calcul/justification |
|---|---|
| Méthode d'exposition (par exemple : dérive, réentrée, contact avec le sol, consommation des récoltes ou de l'eau potable, résidus de végétaux) |
- |
| Taux d'application | - |
| Aire d'application | - |
| Fréquence d'exposition | - |
| Milieux d'application (p. ex., agriculture, serres, résidences) | - |
| Délais de réentrée | - |
| Voies d'exposition prévues (par exemple : voie cutanée et inhalation) basée sur la méthode d'application, le produit et les propriétés physicoâ€'chimiques constituantes |
- |
| Concentration dans des milieux environnementaux (ppm) (au besoin) | Le dépassement des critères de classification de la persistance (annexe 4) doit être pris en compte dans ce calcul |
| Estimation de l'exposition, α (mg/kg pc/j) | Présenter le calcul, indiquer le modèle utilisé et les hypothèses de modélisation associées |
| - | Hypothèse/calcul/justification |
|---|---|
| Effet critique et dose critique, β (mg/kg pc/j) et/ou Coefficient de pouvoir cancérogène, ql* (mg/kg pc/j)-1 |
Tels qu'indiqués à l'annexe 4 |
| Marge d'innocuité (β/α) et/ou Risque additionnel de cancer (RAC) (q1* x α) | - |
Environnement
| - | Hypothèse/calcul/justification |
|---|---|
| Milieu cible prévu (par exemple : sol, air, milieu aquatique, sédiments) basée sur la méthode d'application, le produit et les propriétés physicoâ€'chimiques des ingrédients |
- |
| Méthodologie et équipement d'application | - |
| Taux d'application | - |
| Fréquence d'application | - |
| Estimation de la concentration dans le milieu environnemental, γ (ppm) (par exemple : concentration dans le milieu aquatique, dans les sédiments, dans le sol et dans les granules imprégnées) |
Présenter le calcul, indiquer le modèle utilisé et les hypothèses de modélisation associées Le dépassement des critères de classification de la persistance et/ou de bioaccumulation, bioconcentration ou bioamplification (annexe 4) doit être pris en compte dans ce calcul |
| Estimation de l'exposition des organismes préoccupants, δ (mg/kg pc/j) (le cas échéant, par exemple toxicité chez les vertébrés aviaires et terrestres) |
Présenter le calcul, indiquer le modèle utilisé et les hypothèses de modélisation associées (p. ex., taux d'ingestion journalier de sol ou de granules) |
| - | Hypothèse/calcul/justification |
|---|---|
| Les organismes préoccupants et les concentrations environnementales critiques connexes, ε (ppm) | Tels qu'indiqués à l'annexe 4 |
| Les organismes préoccupants et les doses critiques connexes, ζ (mg/kg pc/j) (le cas échéant, p. ex., toxicité chez les vertébrés aviaires et terrestres) |
Tels qu'indiqués à l'annexe 4 |
| Quotient de risque (ε/γ) | - |
| Marge de sécurité (ζ/δ) (le cas échéant, p. ex., toxicité chez les vertébrés aviaires et terrestres) |
- |
ε L'effet critique, correspond d'ordinaire au premier effet nocif à survenir dans la base de données sur la toxicité lorsqu'on augmente la dose. La dose critique est la dose qui produit l'effet critique observé.
Annexe 6 : Caractérisation du danger microbien (liste de vérification)
Cette liste de vérification est destinée à faciliter la classification des risques dans différents contextes biologiques et d'exposition.
| Danger | Organisme | Oui/Non | Références |
|---|---|---|---|
| Pathogénicité / Toxicité | Humains | - | - |
| Mammifères | - | - | |
| Autres vertébrés terrestres (par exemple les oiseaux) | - | - | |
| Plantes et cultures terrestres | - | - | |
| Invertébrés terrestres (par exemple, abeilles, vers de terre, collemboles) | - | - | |
| Vertébrés aquatiques (poissons) | - | - | |
| Invertébrés aquatiques (benthiques, épibenthiques) | - | - | |
| Plantes aquatiques (algues) | - | - | |
| Toxigénicité Note de tableau a | - | - | |
| Sensibilisation/Irritation | Humains | - | - |
| Mammifères | - | - | |
| Autres vertébrés terrestres (par exemple, les oiseaux) | - | - | |
| Potentiel dermatophytique | Humains | - | - |
| Mammifères | - | - | |
| Toxigénicité Note de tableau a | Humains | - | - |
| Mammifères | - | - | |
| Autres vertébrés terrestres (par exemple les oiseaux) | - | - | |
| Altération après récolte | Plantes et cultures terrestres | - | - |
| Inhibition de la croissance | Plantes et cultures terrestres | - | - |
| Danger | Organisme | Oui/Non | Références |
|---|---|---|---|
| Résistance aux antimicrobiens importants sur le plan médical Note de tableau a | Microorganismes | - | - |
| Libération de gènes de résistance aux antimicrobiens Note de tableau a | Microorganismes | - | - |
Annexe 7 : Caractérisation de l'exposition à un microorganisme – facteurs à considérer
Cette annexe décrit les principaux facteurs biologiques, écologiques et liés à l'utilisation afin d'aider les demandeurs à évaluer l'exposition microbienne.
| Catégorie | Références |
|---|---|
| Répartition géographique du micro-organisme | - |
| Habitats naturels : sol, eau, air ou organismes vivants (par exemple, endophyte, épiphyte) | - |
| Relations avec l'hôte : symbiotiques, saprophytes ou pathogènes | - |
| Présence sur les cultures alimentaires/fourragères dans des environnements naturels | - |
| Résidus dans les denrées alimentaires/aliments pour animaux : accumulation du micro-organisme ou de ses métabolites dans les parties comestibles des plantes Note de tableau a | - |
| Catégorie | Références |
|---|---|
| Paramètres de croissance : température, pH, conditions osmotiques (minima, maxima, optima) | - |
| Caractéristiques nutritionnelles et métaboliques : besoins en oxygène, sources d'énergie | - |
| Sensibilité aux antibiotiques, aux métaux, à la lumière du soleil et à la dessiccation | - |
| Conditions favorables à la production de toxines Note de tableau a | - |
| Catégorie | Références |
|---|---|
| Formes au cours du cycle de vie : cellules motiles, kystes dormants, spores | - |
| Mécanismes de reproduction et de dispersion | - |
| Stratégies de survie dans des conditions défavorables | - |
| Potentiel de dispersion des caractères génétiques ou du transfert de gènes (obligatoire pour les microorganismes modifiés par des techniques biologiques moléculaires) | - |
| Catégorie | Références |
|---|---|
| Caractères spécifiques à la souche qui diffèrent des caractéristiques typiques de l'espèce (obligatoire pour les souches génétiquement modifiées) | - |
| Catégorie | Références |
|---|---|
| Cultures/plantes destinées à l'application | Étiquette |
| Méthode et équipement d'application | Étiquette |
| Dose et fréquence d'application | Étiquette |
| Voies d'exposition prévues : cutanée, inhalation, ingestion | - |
Annexe 8 : Considérations relatives à la classification de la gravité du danger microbien et du niveau d'exposition
Les demandeurs peuvent utiliser cette annexe pour déterminer la classification des dangers d'un micro-organisme en examinant 2 facteurs clés :
- gravité du danger – Décrit le degré de toxicité du micro-organisme pour :
- les êtres humains
- les animaux
- les plantes
- l'environnement
- Niveau d'exposition – Décrit la probabilité que le micro-organisme soit
- libéré
- se propage
- affecte les populations sensibles
En comparant les caractéristiques de leur micro-organisme aux descriptions figurant dans les catégories de risque élevé, moyen et faible, les demandeurs peuvent identifier la classification la plus appropriée.
| Classification | Considérations relatives à la classification | |
|---|---|---|
| Gravité du danger | Niveau d'exposition | |
| Élevé |
|
|
| Moyen |
|
|
| Faible |
|
|
Source : Adapté de Environnement Canada et Santé Canada (2011) : Cadre d'évaluation scientifique des risques liés aux microorganismes réglementés en vertu de la Loi canadienne sur la protection de l'environnement (1999)
Remarque : es combinaisons de facteurs au sein de chaque catégorie de gravité du danger ou du niveau d'exposition sont possibles et pourraient affecter l'ensemble de l'évaluation du danger ou de l'exposition.
Annexe 9 : Exigences en matière d'étiquetage pour les engrais-pesticides autorisés pour un usage domestique ou de jardinage
- Les titres ou mentions en caractères gras doivent figurer sur l'étiquette, mais ne doivent pas nécessairement être imprimés en caractères gras. Les autres mentions sont recommandées, mais ne sont pas obligatoires
- Le texte en majuscules doit être en majuscules sur l'étiquette, sauf indication contraire
- Il est recommandé d'utiliser la formulation exacte de toutes les mentions, mais cela n'est pas obligatoire tant que le sens est le même. Aucune information contradictoire ne doit figurer sur l'étiquette
- Le texte entre crochets [ ] fournit des renseignements supplémentaires et ne devrait pas figurer sur l'étiquette
| NOM COMMUN : | FARINE DE GLUTEN DE MAÏS |
|---|---|
| ANALYSE GARANTIE : | Farine de gluten de maïs (réelle) |
| UTILISATION APPROUVÉE : | Dans les engrais spéciaux pour pelouses et gazons contenant des constituants d'engrais compatibles. |
| ALLÉGATIONS APPROUVÉES : |
|
| TAUX D'APPLICATION : | 9500 - 9800 g de farine de gluten de maïs / 100 m2 |
| MODE D'EMPLOI : |
|
| PRÉCAUTIONS : |
|
| PREMIERS SECOURS : |
|
| INFORMATIONS TOXICOLOGIQUES : | Traiter en fonction des symptômes. |
| ENTREPOSAGE : | Conserver dans un endroit frais et sec, à l'écart des semences, des engrais et autres pesticides. Conserver ce produit à l'écart des aliments et des aliments pour animaux. Tenir à l'écart du feu, des flammes nues et de toute autre source de chaleur. |
| ÉLIMINATION : | Ne réutilisez pas le contenant vide. Jetez le contenant vide avec les ordures ménagères. Les produits inutilisés ou partiellement utilisés doivent être éliminés dans des sites d'élimination des déchets dangereux désignés par la province ou la municipalité. |
| AVIS À L'UTILISATEUR : | Ce produit doit être utilisé conformément aux instructions figurant sur l'étiquette. L'utilisation de ce produit dans des conditions dangereuses constitue une infraction à la Loi sur les produits antiparasitaires. |
| INGRÉDIENTS ACTIFS DE PESTICIDES COMPATIBLES ACCEPTÉS : | AUCUN |
| MARQUES APPROUVÉES DE PRODUITS PESTICIDES : | Voir la section sur la farine de gluten de maïs des marques approuvées par l'ARLA des produits pesticides |
| NOM COMMUN : | SULFATE FERREUX |
|---|---|
| ANALYSE GARANTIE : | Sulfate ferreux (réel) |
| UTILISATION APPROUVÉE : | Dans les engrais spéciaux pour pelouses et gazons contenant des constituants d'engrais compatibles. |
| ALLÉGATIONS APPROUVÉES : | Contrôle la mousse dans les pelouses. |
| DOSAGES D'APPLICATION : | 250 à 980 g de sulfate ferreux / 100 m2 |
| MODE D'EMPLOI : |
|
| PRÉCAUTIONS : |
|
| PRÉCAUTIONS ENVIRONNEMENTALES : |
|
| PREMIERS SOINS : |
|
| ÉLIMINATION : | Jeter le contenant vide dans les ordures ménagères. |
| INGRÉDIENTS ACTIFS PESTICIDES COMPATIBLES ACCEPTÉS : | AUCUNE |
| MARQUES APPROUVÉES DE PRODUITS PESTICIDES : | Consultez la section sur le sulfate ferreux Marques de produits antiparasitaires approuvées par l'ARLA |
Annexe 10 : Ressources - Toxicologie
Ressources canadiennes
- Centre canadien d'hygiène et de sécurité au travail (CCHST)
- Commission des normes, de l'équité, de la santé et de la sécurité du travail (CNESST)
Environnement et Changement climatique Canada
Santé Canada
- Évaluation des substances de la première Liste des substances d'intérêt prioritaire (LSIP1)
- Évaluation des substances de la deuxième Liste des substances d'intérêt prioritaire (LSIP2)
Ressources internationales
Nations Unies
- Organisation des Nations Unis pour l'alimentation et l'agriculture (FAO). Codex Alimentarius
- Programme International sur la Sécurité des Substances Chimiques. INCHEM (en anglais seulement)
États-Unis
- Agency for Toxic Substances and Disease Registry (ATSDR), Toxic Substances Portal (en anglais seulement)
- Centers for Disease Control and Prevention (CDC), The National Institute for Occupational Safety and Health (NIOSH) (en anglais seulement)
- Department of Commerce, National Institute of Standards and Technology (NIST), NIST Chemical WebBook, SRD 69 (en anglais seulement)
- Environmental Protection Agency (EPA), Ecotox (en anglais seulement)
- Environmental Protection Agency (EPA), Integrated Risk Information System (en anglais seulement)
- National Library of Medicine, Toxicological Data Network: ChemIDplus (en anglais seulement)
Annexe 11 : Ressources – Microbiologie
Ministères et organismes canadiens
Agence canadienne d'inspection des aliments (ACIA)
Agriculture et Agroalimentaire Canada (AAC)
Environnement et Changement climatique Canada
- Guide des essais de pathogénicité et de toxicité de nouvelles substances microbiennes pour les organismes aquatiques et terrestres
- Document d'orientation sur les méthodes statistiques pour les essais de toxicité environnementale / [publié par] la Section du développement et des applications des méthodes, Centre de technologie environnementale, Environnement Canada.
- Environnement Canada. Janvier 2022. Liste intérieure des substances (contient plusieurs micro-organismes du groupe de risque 2).
- Cadre d'évaluation des risques microbiens (CERM) en vertu du Règlement sur les renseignements concernant les substances nouvelles (organismes) de la Loi canadienne sur la protection de l'environnement (1999) avril 2024 https://www.canada.ca/fr/environnement-changement-climatique/services/gestion-pollution/evaluation-substances-nouvelles/biotechnologie-organismes-vivants/cadre-evaluation-risques-microbiens.html
Santé Canada/Agence de la santé publique du Canada
- Fiche Technique Santé-Sécurité : Agents Pathogènes
- ePATHogène - la base de données sur les groupes de risque
- Catégorisation des médicaments antimicrobiens basée sur leur importance en médecine humaine
- Système canadien de surveillance de la résistance aux antimicrobiens (SCSRA)
Ressources internationales
- American Type Culture Collection (ATCC) (en anglais seulement)
- DSMZ (Allemagne) – Deutsche Sammlung von Mikroorganismen und Zellkulturen
- American Type Culture Collection ATCC Mycology Collection
- The United States Department of Agriculture (USDA) Fungal Databases
- The United States Department of Agriculture (USDA) ARS Culture Collection (NRRL)
- European Food Security Authority EFSA Guidance on Risk Assessment of Genetically Modified Microorganisms